HSR voor laterale elleboog tendinopathie

Inleiding
Er bestaan verschillende behandelingen voor laterale elleboog tendinopathie, ook wel laterale epicondylalgie genoemd. Het is moeilijk voor de clinicus om mensen te informeren over de beste beschikbare behandeling, zowel vanuit het perspectief van pijn en functionele verbetering als vanuit het perspectief van structurele integriteit, omdat er onzekerheid bestaat over de superieure behandelcombinaties. Tot de meest voorkomende behandelopties in de fysiotherapiepraktijk behoren zware langzame weerstandstraining (HSR) en tendon dry needling. Deze opties worden vaak aangevuld met corticosteroïde injecties.
Terwijl studies naar geïsoleerde progressieve weerstandstraining, zoals HSR, superieure korte- en langetermijneffecten hebben aangetoond bij patella- en achillestendinopathie, waren de resultaten voor laterale elleboog tendinopathie tegenstrijdig. Het blijft ook onbekend of een corticosteroïde injectie of dry needling in combinatie met een HSR-programma superieur is aan een HSR-programma alleen voor laterale elleboog tendinopathie. Daarom werd de huidige studie opgezet.
Methoden
Deze studie behandelt een kritieke vraag in de behandeling van laterale elleboog tendinopathie: of het toevoegen van corticosteroïde injecties (CSI) of tendon needling (TN) aan een trainingsprogramma met zware langzame weerstand (HSR) superieure resultaten biedt in vergelijking met HSR alleen.
In Denemarken werd een 3-arms gerandomiseerd, dubbelblind, placebogecontroleerd onderzoek uitgevoerd om de effecten te onderzoeken van heavy slow resistance (HSR)-training in combinatie met ofwel een corticosteroïdeninjectie (CSI), tendon dry needling (TN) of placebo needling (PN) voor chronische unilaterale laterale elleboog tendinopathie.
De studie omvatte volwassenen van 18 tot 70 jaar die gedurende ten minste drie maanden symptomen van een laterale elleboog tendinopathie hadden. De belangrijkste diagnostische criteria waren klinische symptomen van pijn in de laterale elleboog en/of onderarm en gevoeligheid bij palpatie van de epicondylus humerus lateralis. Deze klinische symptomen moesten worden gereproduceerd in ten minste twee van de drie specifieke tests:
- Cozen test
- Maudsley-test
- onderarm supinatie test
Verder werd de Disabilities of the Arm, Shoulder and Hand (DASH) score ingevuld op baseline. De vereiste voor inclusie was een DASH score van meer dan 30 punten. Naast de klinische vereisten was ultrasonografisch bewijs van toegenomen peesdikte, hypo-echoïsche signalen of pathologische power Doppler-activiteit binnen de oorsprong van de gemeenschappelijke strekpees nodig voordat iemand in aanmerking kwam voor inclusie.
Patiënten met eerdere fracturen, artrose, bilaterale symptomen, systemische artritis, diabetes of patiënten die binnen de voorgaande drie maanden een CSI of dry needling hadden ontvangen, werden uitgesloten.
De primaire uitkomst was de DASH-score, die de functie en symptomen van de bovenste extremiteit beoordeelt, na 52 weken (1 jaar). Deze vragenlijst bevat 30 vragen over functioneren en symptomen in de afgelopen week, gewaardeerd van 1 tot 5. De totale score loopt van 0 (geen beperking) tot 100 (ernstige beperking). De totaalscore loopt van 0 (geen beperking) tot 100 (ernstige beperking).
- Een DASH score onder de 15 punten wijst op geen probleem, terwijl 16-40 punten wijzen op een probleem, maar de persoon is nog steeds in staat om te werken. Scores boven de 40 punten betekenen een onvermogen om te werken en aanzienlijke functionele problemen. Er is voorgesteld dat een DASH score onder de 30 punten betekent dat patiënten hun aandoening aan de bovenste extremiteit niet langer als een probleem beschouwen. Een score tussen 10-29 punten is een benchmark voor terugkeer naar werk, waarbij patiënten zich bewust zijn van beperkingen maar deze niet als problematisch beschouwen. Het minimale klinisch belangrijke verschil voor de DASH score is 12 punten.
Secundaire uitkomsten waren onder andere de verkorte QuickDASH score, pijnintensiteit gemeten door een 11-punts Numerical Rating Scale (NRS), pijnvrije grijpkracht (gemeten met een digitale handdynamometer) en hypervascularisatie (beoordeeld door power Doppler ultrasonografie). Deze werden gemeten bij baseline, 12, 26 en 52 weken.
Interventies
Elke geïncludeerde deelnemer kreeg een "injectie", die werd gevolgd door een 12 weken durend HSR-protocol.
Aangezien er 3 groepen waren, werden er drie verschillende "injecties" gebruikt
- Corticosteroïd injectie (CSI): 1 ml Depo-Medrol (40 mg/ml) en 1 ml lidocaïne (10 mg/ml) geïnjecteerd onder de aangedane pees, geleid door echografie.
- Tendon Needling (TN): De naald werd op 2-3 plaatsen door de aangedane pees gestoken, gecombineerd met een injectie van 1 ml 0,9% isotone zoutoplossing, geleid door echografie.
- Placebo naaldbehandeling (PN): 1 ml 0,9% isotone zoutoplossing net onder de huid geïnjecteerd, waarbij ervoor wordt gezorgd dat er geen contact is met de pees, geleid door echografie.
Belangrijke opmerking: Voor alle injecties werd de spuit afgedekt en werd het ultrasone scherm verborgen voor de deelnemer om blindering te garanderen.
Vervolgens begon elke deelnemer na de injectie met het Heavy Slow Resistance (HSR)-trainingsprogramma, met een verplichte rustperiode van twee dagen na de injectie. Het programma werd drie keer per week thuis uitgevoerd, met minimaal één dag rust tussen de sessies.
Oefeningen: Het programma bestond uit drie verschillende oefeningen gericht op extensie, flexie en supinatie/pronatie van de hand, aangepast aan de principes die gebruikt worden voor patellapees- en achillestendinopathie. De trainingsbelasting werd progressief verhoogd met behulp van elastische banden met variërende weerstand:
- Week 1: 3 sets van de maximale 15 herhalingen (RM) voor elke oefening.
- Weken 2-3: 3 sets van 12 RM.
- Weken 4-5: 3 sets van 10 RM.
- Weken 6-8: 3 sets van 8 RM.
- Na week 8: 3 sets van 6 RM.
Alle oefeningen werden langzaam uitgevoerd, met drie tot vier seconden in elke richting (concentrische en excentrische fasen). Tussen elke set werd twee minuten rust ingelast.
Patiënten kregen de instructie dat pijn tot 5 op 10 op de NRS acceptabel was tijdens en na HSR, als deze kort na de oefening afnam of als de belasting werd aangepast. Ze kregen ook het advies om andere activiteiten of oefeningen te vermijden die de pijn boven dit niveau deden toenemen. Er werd een trainingsdagboek gebruikt om de progressie bij te houden. Een controlebezoek aan een fysiotherapeut in week 4 zorgde voor een correcte uitvoering en progressie van de oefeningen.
Resultaten
Een totale steekproef van 58 deelnemers werd geanalyseerd, met 21 deelnemers in de CSI groep, 17 in de dry needling groep en 20 in de placebo needling groep. Bij aanvang waren de groepen volgens de auteurs gelijk wat betreft demografische gegevens, duur van de symptomen, activiteitenniveaus en primaire en secundaire uitkomstmaten.
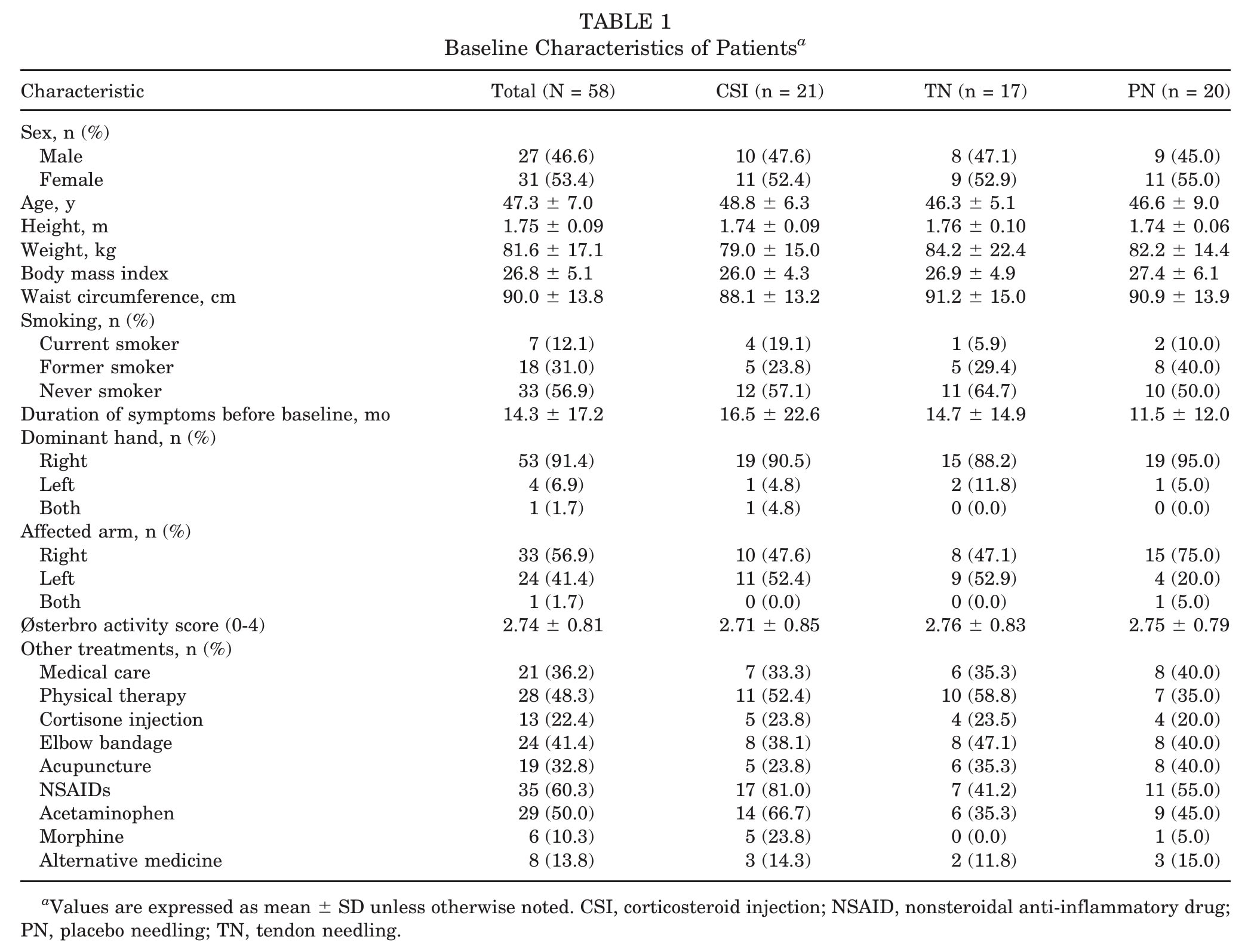
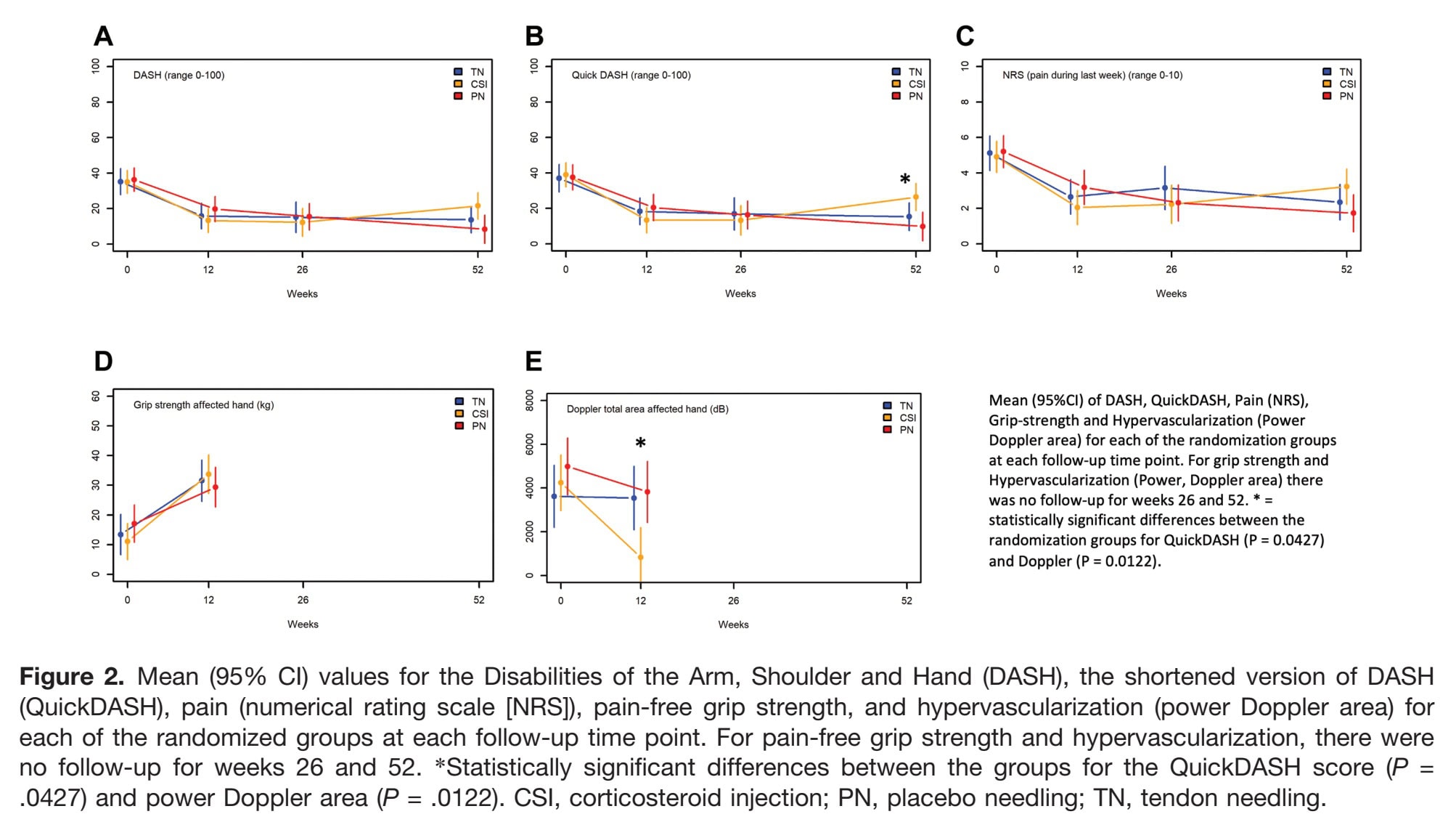
Vergelijkingen binnen de groepen toonden aan dat alle groepen na 12, 26 en 52 weken verbeterden op alle patiëntgerapporteerde uitkomsten (DASH, QuickDASH, NRS). Pijnvrije grijpkracht verbeterde van uitgangswaarde tot 12 weken voor alle groepen en hypervascularisatie nam duidelijk af in de CSI-groep maar niet in de PN- en TN-groepen.
De effecten tussen de groepen lieten geen significante algemene verschillen zien in DASH-verbeteringen na 12 of 26 weken. Na 52 weken bereikte de algemene vergelijking nog steeds geen statistische significantie (p=.0581), maar uit paarsgewijze analyses (Tabel 2) bleek dat de CSI-groep significant hogere (slechtere) DASH-scores had vergeleken met de PN-groep (p=.0176).
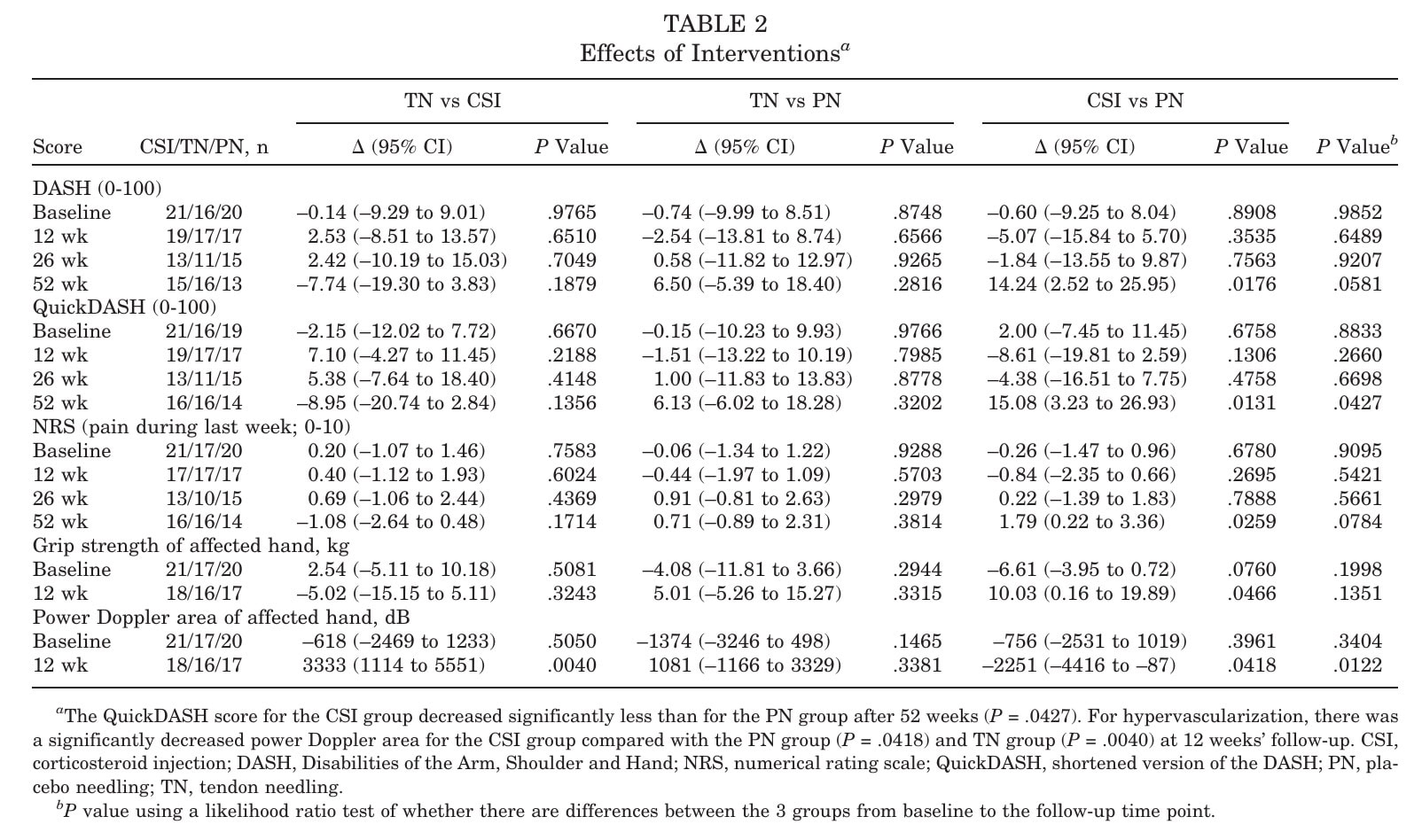
Secundaire uitkomsten
De QuickDASH na 52 weken vertoonde hetzelfde patroon als de DASH, met significant slechtere scores in de CSI-groep vergeleken met PN (p=.0427).
Voor pijn (NRS) werden geen verschillen waargenomen tussen de groepen na 12 of 26 weken. Na 52 weken rapporteerde de CSI-groep meer pijn dan de PN-groep (paarsgewijs p=.0259), hoewel de algemene test voor alle drie groepen niet significant was. Dit suggereert dat het langetermijneffect van CSI nadelig kan zijn in vergelijking met HSR plus placebo.
Kortetermijnvoordelen werden na 12 weken waargenomen in de CSI-groep, met significant hogere grijpkracht in vergelijking met PN (p=,0466), naast een sterke afname van hypervasculisatie. Deze structurele en krachtveranderingen vertaalden zich echter niet in blijvend klinisch voordeel.
De auteurs analyseerden ook de gebied onder de curve (AUC) voor DASH over alle tijdspunten (baseline, 12, 26, 52 weken) en vonden geen algemene verschillen tussen de groepen. Dit verklaart waarom ze de algemene gelijkenis tussen groepen benadrukken, ondanks de 52-weekse paarsgewijze effecten. Belangrijk is dat de verslechtering die werd gezien in de CSI-groep niet alleen statistisch significant was, maar ook klinisch betekenisvol (≥MCID drempelwaarden).
Samenvattend verbeterden alle deelnemers met HSR voor laterale elleboog tendinopathie, ongeacht aanvullende interventie. CSI was echter geassocieerd met slechtere zelfgerapporteerde functie en pijn op de lange termijn.
Questions and thoughts
Moeten we nu HSR voorschrijven voor laterale elleboog tendinopathie voor elke patiënt? Dit onderzoek is een sterke ondersteuning van HSR als eerstelijns strategie: het leverde consistente, klinisch betekenisvolle verbeteringen op voor alle uitkomsten. Toch kunnen patiënten met acute pijn om een "snelle oplossing" vragen. Hoewel corticosteroïde injecties de hypervasculisatie kunnen verminderen en veranderingen op korte termijn kunnen geven, toonde dit onderzoek aan dat CSI de pijn en functie na 52 weken verslechterde. Patiënten moeten over dit risico worden geïnformeerd wanneer zij CSI overwegen.
Alle deelnemers verbeterden binnen de groepen, wat de waarde van HSR voor laterale elleboog tendinopathie versterkt. De studie niet gecorrigeerd voor meervoudige vergelijkingeneen beperking die door de auteurs wordt erkend. Dit betekent dat sommige statistisch "positieve" paarsgewijze bevindingen (bijv. grijpkracht na 12 weken) met voorzichtigheid moeten worden geïnterpreteerd.
Een ander punt is hypervascularisatie: alleen de CSI-groep liet een duidelijke vermindering zien, maar dit werd niet weerspiegeld in de functionele uitkomsten. Dit benadrukt een bredere kwestie - veranderingen in structurele beeldvorming komen niet noodzakelijk overeen met door de patiënt gerapporteerde uitkomsten, en functionaliteit kan belangrijker zijn dan het oplossen van pathologie.
De naleving van het HSR-programma was uitstekend: deelnemers voltooiden 83% van de sessies (gemiddeld 269/324). Dat is opmerkelijk voor een programma met zware belasting, wat suggereert dat de zorgvuldige instructie en monitoring door de fysiotherapeuten cruciaal waren. Een haalbaarheidsstudie van Sveinall et al. (2024) rapporteerden slechts 32% therapietrouw bij HSR zonder toezicht, vanwege pijnverergering. Dit onderstreept dat HSR goed kan werken, maar alleen als patiënten worden ondersteund en voorgelicht.
Talk nerdy to me
De randomisatie was gestratificeerd op basis van geslacht en baseline DASH-score. Deelnemers, statistici, onderzoeksassistenten en fysiotherapeuten waren geblindeerd; alleen de onderzoeksartsen kenden de toewijzingen. Toch was de blindering niet perfect: 52% van de CSI- en 58% van de PN-deelnemers gokten correct, hoger dan de 33% die op basis van toeval werd verwacht. Dit kan de door de patiënt gerapporteerde uitkomsten vertekend hebben.
Hoewel de groepen bij aanvang als gelijk werden gerapporteerd, was het gebruik van pijnmedicatie ongelijk. Er werd bijvoorbeeld 23,8% morfine gebruikt in de CSI-groep, maar slechts 5% in de PN-groep. Het gebruik van NSAID's en acetaminofen was ook hoger bij CSI. Deze onevenwichtigheid bedreigt interne validiteitHet gebruik van morfine zou de manier waarop deelnemers pijn waarnamen of rapporteerden kunnen veranderen, waardoor mogelijk interventie-effecten worden gemaskeerd of opgeblazen. Hoewel randomisatie bedoeld is om dergelijke factoren in evenwicht te brengen, kunnen toevallige onevenwichtigheden in kleine onderzoeken de resultaten beïnvloeden.
Ik merkte enkele schijnbare tegenstrijdigheden op tussen algemene en paarsgewijze vergelijkingen. Ter verduidelijking:
- Algemene tests (zoals ANOVA of gemengde modellen over alle groepen) vragen of alle drie groepen samen verschillen. Hier werden geen algemene verschillen gevonden na 52 weken voor DASH, QuickDASH of NRS.
- Paargewijze tests kijken naar specifieke contrasten (CSI vs PN, CSI vs TN, TN vs PN). Deze lieten significante verschillen zien, bijv. CSI vs PN na 52 weken.
- Deze discrepantie ontstaat doordat algemene tests minder sterk zijn om geïsoleerde groepsverschillen te detecteren en doordat meervoudige paarsgewijze tests het risico op type I fouten vergroten. De auteurs hebben niet gecorrigeerd voor meervoudige vergelijkingen, wat de interpretatie verder bemoeilijkt.
Het rapportageprobleem is dat de tekst soms de nadruk legt op "geen verschillen" terwijl de tabellen significante p-waarden per paar tonen (bijv. CSI vs PN grijpkracht op 12 weken, p=.0466). Zonder te verduidelijken of er aanpassingen zijn gedaan, kan dit misleidend zijn. Volgens CONSORT moeten alle significante resultaten transparant worden gerapporteerd. De auteurs erkenden het risico van een opgeblazen type I fout, maar lieten het aan de lezer over om aanpassingen te maken - geen ideale werkwijze.
Tot slot vroegen de auteurs zich zelf af of de DASH gevoelig genoeg is voor deze aandoening. Ze merkten op dat de Patient-Rated Tennis Elbow Evaluation een meer specifiek instrument zou zijn geweest, maar het ontbrak aan een gevalideerde Deense versie. Deze beperking kan hun vermogen om subtiele maar echte verschillen tussen de groepen te detecteren hebben beperkt.
Boodschappen die je mee moet nemen
Voor mensen met een laterale elleboog tendinopathie lijkt een thuisgebaseerd Heavy Slow Resistance (HSR) trainingsprogramma met eenvoudige elastiekoefeningen effectief te zijn in het verbeteren van symptomen en functie op zowel de korte als lange termijn. Het toevoegen van corticosteroïde injecties (CSI) of dry needling van de pezen (TN) aan dit HSR-programma verbeterde de voordelen niet en leek, in het geval van CSI's, een negatieve invloed te hebben op de door de patiënt gerapporteerde uitkomsten op de lange termijn. Daarom kan een focus op HSR-training in combinatie met goede instructies over pijnniveaus en progressie de meest gunstige aanpak zijn.
Referentie
Bekijk twee 100% Gratis Webinars over Schouderpijn en Ulna-zijde Polspijn
Verbeter je klinische redenering voor het voorschrijven van oefeningen bij de actieve persoon met schouderpijn met Andrew Cuff en navigeer door de klinische diagnose en behandling met een casestudie van een golfer door Thomas Mitchell

