Auswirkung mechanischer Belastung auf die ANPASSUNG der Sehne - Biologische Hintergründe für präzise Bewegungstherapie-Interventionen
Einführung
Trotz der Fortschritte in unserem Verständnis der Pathogenese der Tendinopathie sind die Ergebnisse nach herkömmlichen konservativen und medikamentösen Eingriffen nach wie vor uneinheitlich, und viele Patienten leiden unter anhaltenden Schmerzen und Funktionseinschränkungen. Das viel zitierte Kontinuumsmodell von Jill Cook legt nahe, dass der degenerative Anteil einer Sehne strukturell irreversibel ist. Neue strukturelle und mechanobiologische Evidenzen stellen diese Annahme jedoch in Frage und weisen darauf hin, dass das Gewebe der Sehnen möglicherweise eine größere Fähigkeit zur Anpassung und zum Umbau besitzt als bisher angenommen.
Diese Übersichtsarbeit untersucht den Einfluss von mechanischen Belastung auf die ANPASSUNG der Sehne und die biologischen Mechanismen, die der Degeneration zugrunde liegen, mit besonderem Schwerpunkt auf der zellulären Signalübertragung, dem Matrixumbau und den Mechanotransduktionswegen. Durch die Einbeziehung aktueller experimenteller Ergebnisse soll ein biologisch fundierter Rahmen für die Verschreibung von Übungen zur Behandlung von Tendinopathien geschaffen werden. Diese theoretische Synthese dient als Grundlage für eine demnächst erscheinende Übersichtsarbeit, die sich mit hoch belastenden Trainingsstrategien befasst und ein neuartiges Belastungsprotokoll für die klinische Anwendung bei Tendinopathie vorstellt.
Methoden
Diese Übersichtsarbeit fasst die Ergebnisse mehrerer experimenteller Studien zusammen, die überwiegend in Tiermodellen durchgeführt wurden.
Ergebnisse
Biologische Grundlagen des Aufbaus der Sehnen
Kollagen vom Typ I (COL1/Col1a1) ist das wichtigste Strukturprotein von Sehnen und Bändern und verleiht ihnen Zugfestigkeit. Nach einer Verletzung nimmt die Synthese von Kollagen zu; die Matrixablagerung während der proliferativen Phase ist jedoch häufig desorganisiert. Während gesunde Sehnen parallel zu den mechanischen Kräften ausgerichtete Kollagenfibrillen aufweisen, enthalten pathologische Sehnen kleinere, weniger vernetzte und desorganisierte Fibrillen. Obwohl Kollagen vom Typ I im Vergleich zu Kollagen vom Typ III einen höheren mechanischen Widerstand bietet, enthalten heilende Sehnen häufig einen höheren Anteil an Kollagen vom Typ III. Matrix-Metalloproteinasen (MMPs), Enzyme, die für den Abbau von Kollagen verantwortlich sind, sind während des Umbaus von Gewebe gleichzeitig aktiv.
Verletzte erwachsene Sehnen werden typischerweise hochgradig zellulär und entwickeln eine desorganisierte Kollagenmatrix, die durch Fibrillen mit geringem Durchmesser gekennzeichnet ist, was zu einem degenerativen Gewebephänotyp führt.
Regeneration von Gewebe und Rekapitulation der Entwicklung
Als Reaktion auf eine Verletzung werden Gene, die normalerweise während der Embryonalentwicklung aktiv sind, erneut exprimiert. Stamm- und proliferative Zellpopulationen expandieren und differenzieren sich zu spezialisiertem Gewebe; erwachsene Sehnen können sich jedoch im Allgemeinen nicht vollständig regenerieren und hinterlassen oft eine degenerative Restmatrix. Im Gegensatz dazu zeigen neonatale Modelle eine größere Fähigkeit zur funktionellen Reparatur, wobei die Organisation des Gewebes den Entwicklungsprozessen ähnelt. Diese Ergebnisse deuten darauf hin, dass die Regenerationsfähigkeit möglicherweise von der Fähigkeit abhängt, Entwicklungsprogramme zu rekapitulieren, eine Eigenschaft, die bei jüngeren Organen und bestimmten experimentellen Modellen stärker ausgeprägt zu sein scheint als bei der Heilung von Sehnen beim erwachsenen Menschen.
Materialeigenschaften spiegeln mechanische Anforderungen wider
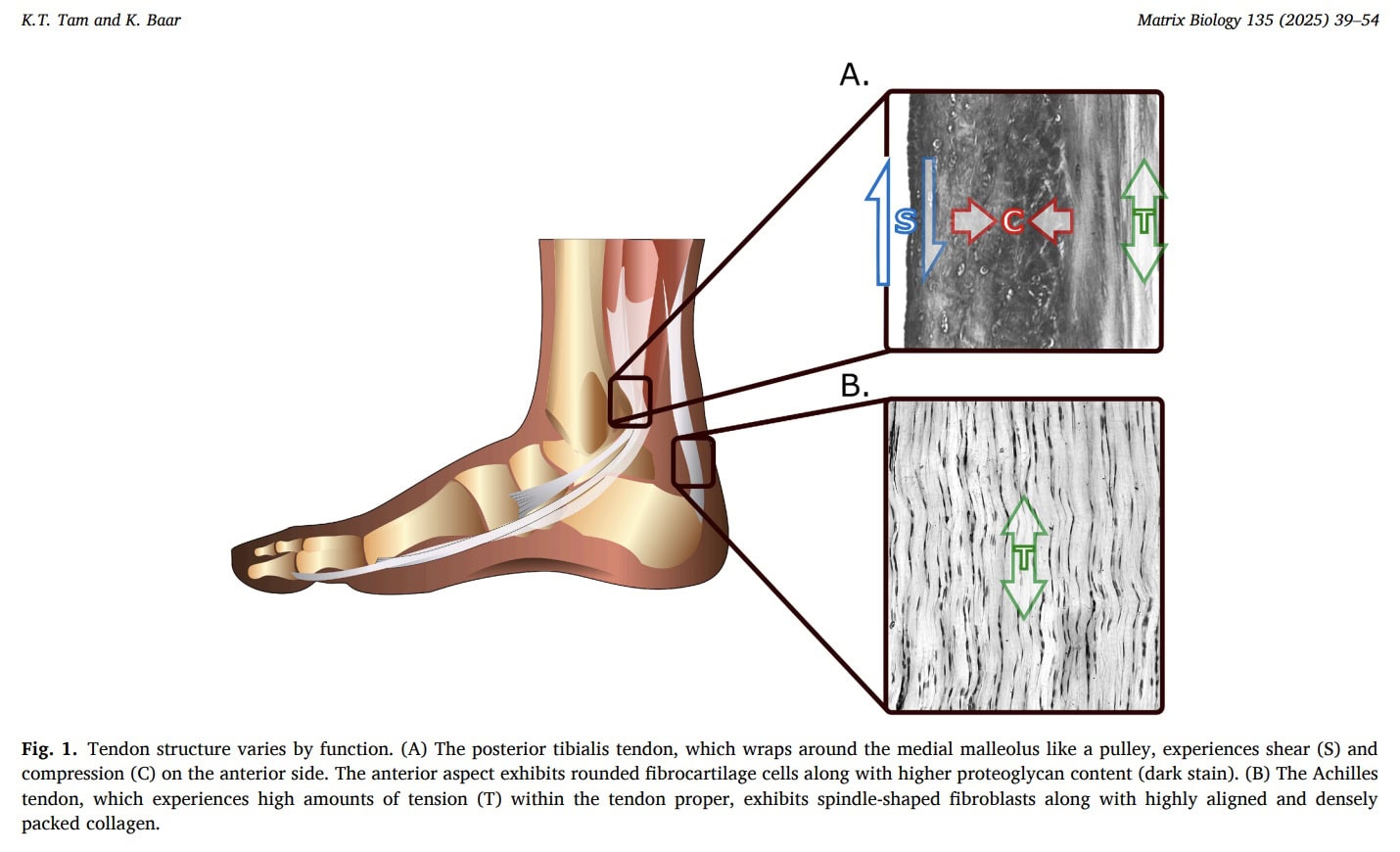
Sehnen können entsprechend ihrer mechanischen Funktion entweder als energiespeichernde oder als positionierende Strukturen kategorisiert werden. Energiespeichernde Sehnen wie die Achilles-Sehne nehmen mechanische Energie auf und geben sie wieder ab, um die Effizienz des Bewegungsapparats zu steigern. Positionierende Sehnen, wie die Tibialis anterior Sehne, positionieren in erster Linie die Gelenke und erleichtern Bewegungen wie das Abrollen des Fußes während des Gehens. Diese funktionellen Unterschiede spiegeln sich in den strukturellen Eigenschaften wider: Energiespeichernde Sehnen besitzen in der Regel eine größere Querschnittsfläche, die die geringere Steifigkeit des Materials kompensiert, um eine elastische Energiespeicherung zu ermöglichen. Sehnen innerhalb der gleichen kinetischen Kette können auch unterschiedliche mechanische Eigenschaften aufweisen. Die Quadrizeps-Sehne und die Patella-Sehne arbeiten beispielsweise in Reihe, weisen aber unterschiedliche Steifigkeitseigenschaften auf, wobei die Quadrizeps-Sehne etwa zweimal weniger steif ist. Dieser Unterschied spiegelt wahrscheinlich ihre mechanischen Umgebungen wider - Ansatz am Knochen für die Patellasehne bzw. Muskel-an-Knochen-Ansatz für die Quadrizeps-Sehne -, die unterschiedliche Belastungsmuster auferlegen und daher die mechanische Belastung der Sehnenanpassung und die Materialanforderungen beeinflussen. mechanische belastung der sehnen anpassung und Materialanforderungen beeinflussen.
Komprimierung
Druckkräfte wirken häufig auf Sehnen ein, insbesondere dort, wo sie sich um knöcherne oder retinakuläre Strukturen wickeln. Experimentelle Studien an Tiermodellen zeigen, dass die Aufhebung der Druckbelastung die Steifigkeit der Sehnen verringert und die strukturelle Anpassung verändert, was darauf hindeutet, dass sich die Sehnen, die einer Kompression ausgesetzt sind, umbauen, um sich an diese mechanische Umgebung anzupassen. Beim Menschen weisen komprimierte Sehnenregionen häufig fibrokartilaginäre Merkmale auf, die reich an Typ-II-Kollagen sind und darauf spezialisiert sind, Druckkräften zu widerstehen.
Schere
Scherkräfte entstehen durch relatives Gleiten zwischen Sehnen, Bändern, Muskeln und angrenzenden Geweben. In der Achilles-Sehne erleichtert das differentielle Gleiten zwischen den Faszikeln die Kraftübertragung, kann aber mit zunehmendem Alter abnehmen, was möglicherweise zu einem reduzierten Bewegungsumfang und einer beeinträchtigten Kraftverteilung beiträgt. Diese Abnahme der Gleitfähigkeit kann teilweise die höhere Häufigkeit von Rupturen der Achillessehne bei älteren Menschen erklären. Wie bei der kompressiven ANPASSUNG kann eine geringere mechanische Belastung zu degenerativen Veränderungen, einem erhöhten Verletzungsrisiko und einer Desadaptation beitragen.
Spezifische Kräfte treiben spezifische molekulare Programme an
Das Zellschicksal und die Zusammensetzung des Gewebes werden stark von der mechanischen Umgebung über Mechanotransduktionswege beeinflusst, was die Bedeutung der folgenden Faktoren unterstreicht mechanischen Belastung auf die ANPASSUNG der Sehne. Mechanische Kräfte lösen biologische und metabolische Anpassungen aus, die die Struktur und Funktion des Gewebes regulieren, obwohl die spezifischen Wege der Heilung von Sehnen noch nicht vollständig verstanden sind. In den folgenden Abschnitten werden die biomechanischen Auswirkungen verschiedener Belastungsmodalitäten auf die Anpassung und Reparatur von Sehnen untersucht.
VERSPANNUNGEN
Manipulationen der mechanischen Umgebung, einschließlich mechanische Belastungist von zentraler Bedeutung für den Umbau der Sehnen und die funktionelle Anpassung. Die Zugbelastung treibt den Umbau des Gewebes voran, doch das Gleichgewicht zwischen nützlichen und potenziell schädlichen Belastungen bleibt kritisch. Ein besseres biomechanisches Verständnis der Belastungsstrategien ist daher für die Optimierung der Rehabilitation und Anpassung der Sehnen unerlässlich.
Scleraxis (Scx) ist ein wichtiger Transkriptionsfaktor, der an der Entwicklung der Sehne und der Regulierung des Kollagens beteiligt ist. Während der Embryogenese fördert Scx die Synthese von Kollagen Typ I (COL1) durch Bindung an regulatorische Regionen des Col1a1-Gens. Seine Expression wird durch die Aktivität des Muskels und die mechanische Belastung beeinflusst. In erwachsenen Sehnen scheint Scx jedoch weniger wichtig für die ANPASSUNG des Wachstums zu sein. Mehrere tenogene Gene - darunter Col1a1, Tenomodulin (Tnmd), Fibromodulin (Fmod) und Mohawk (Mkx) - können als Reaktion auf die Belastung hochreguliert werden, ohne dass sich die Scx-Expression entsprechend verändert. Dies deutet darauf hin, dass die ANPASSUNG der Sehne unabhängig von Scx stattfinden kann und dass seine primäre Rolle eher mit der frühen Fibrillenbildung als mit dem späteren Fibrillenwachstum zusammenhängt. Im Gegensatz dazu scheint Mkx zur Fibrillenvergrößerung und -reifung als Reaktion auf mechanische Stimulation beizutragen, was seine Rolle bei der strukturellen Anpassung der Sehne unterstützt.
Heilende adulte Sehnen weisen häufig Merkmale auf, die entwicklungsbedingtem Gewebe ähneln, darunter Kollagenfibrillen mit kleinem Durchmesser und eine elevierte Scx-Expression. Im Gegensatz zur Embryonalentwicklung reift die Heilungsmatrix jedoch häufig nicht zu organisiertem, belastbarem Gewebe aus. Eine Erklärung dafür ist, dass mechanische Signale möglicherweise nicht ausreichend durch die vernarbte Matrix übertragen werden, ein Phänomen, das mit der Stress-Abschirmung übereinstimmt (siehe unten). Eine beeinträchtigte mechanische Signalübertragung könnte die Aktivierung mechanosensitiver Signalwege wie Mkx verringern, die Reifung von Kollagenfibrillen einschränken und zur Bildung von mechanisch minderwertigem Narbengewebe beitragen.
Komprimierung
Druckkräfte regulieren die Differenzierung von Sehnenzellen und die Zusammensetzung der Matrix. Regionen, die einer Kompression ausgesetzt sind - wie die Enthese und die Sehnenpulleys - entwickeln häufig fibroknorpelähnliche Merkmale, die durch die Expression von Knorpelmarkern wie Col2a1 und Aggrecan gekennzeichnet sind. In der Entwicklung exprimieren Sehnenvorläuferzellen zunächst Scx und Sox9 (einen chondrogenen Transkriptionsfaktor) gemeinsam, bevor sie sich in an Verspannungen angepasste Sehnenzellen und an Kompression angepasste Faserknorpelzellen aufspalten. Experimentelle Evidenzen zeigen, dass anhaltende Kompression die Bildung von knorpelähnlichem Gewebe innerhalb der Sehne induzieren kann, während Zugbelastung die sehnenspezifische Genexpression fördert und chondrogene Pfade unterdrückt. In Abwesenheit von Mkx kann die Zerrung paradoxerweise die chondrogene Genexpression begünstigen, was zur ektopischen Bildung von Faserknorpel führt. Diese Ergebnisse deuten darauf hin, dass Sehnenzellen ein multipotentes Potenzial besitzen und dass die mechanische Belastung die Differenzierung durch spannungs- und druckempfindliche Transkriptionsprogramme steuert.
Scheren
Lubricin und Hyaluronsäure sind wichtige Vermittler des Gleitens der Sehnenfaszikel und des Widerstands gegen Scherkräfte. Ihre biologische Regulierung und ihre Reaktion auf mechanische Belastung sind jedoch noch unzureichend charakterisiert, was das Verständnis ihrer Rolle in der Pathologie und Anpassung der Sehnen einschränkt.
Räumliche Anordnung
Die Organisation des Kollagens ist für die Funktion der Sehne unerlässlich und wird stark durch mechanische Verspannungen reguliert. Während der Entwicklung richten Zugkräfte Zellen und Kollagenfibrillen durch spezialisierte Strukturen (Fibripositoren) aus, wodurch die für gesunde Sehnen charakteristische parallele Architektur entsteht. Selbst in azellulären Kollagenmatrizen kann eine ZERRUNG die Fibrillenausrichtung und -dichte erhöhen, und diese Veränderungen können auch nach der Entlastung anhalten. Die Dauerhaftigkeit des Umbaus hängt jedoch von der Matrixvernetzung ab, die die Anpassungsfähigkeit in alternden oder metabolisch veränderten Geweben, wie z. B. bei Diabetes, verringern kann. Zugbelastungen erhöhen auch den Widerstand gegen den Abbau von Kollagen und aktivieren biochemische Signalwege (einschließlich Mkx), die die Fibrillenreifung unterstützen. Die ANPASSUNG DER SEHNE spiegelt also das Zusammenspiel von passiver mechanischer Ausrichtung und aktiver zellulärer Signalgebung als Reaktion auf mechanischer Belastungein Prozess, der die strukturelle Umgestaltung und die funktionelle Optimierung steuert.
Fehlende und abweichende Kräfte spielen eine Rolle bei der Degeneration von Sehnen und Bändern
Heilende Sehnen ähneln oft unreifem oder embryonalem Gewebe und weisen eine elevierte Scx-Expression, vermehrte fibrillogene Kollagene (III, V, XI), Kollagenfibrillen mit kleinem Durchmesser, eine hohe Zellularität, Vaskulärisierung und das Vorhandensein von Scx+/Sox9+ Vorläuferzellen auf. Diese Merkmale deuten darauf hin, dass die verletzte Sehne zwar ein Entwicklungsprogramm reaktiviert, aber die Progression zur vollständigen mechanischen Reifung nicht erreicht, was wahrscheinlich auf eine veränderte mechanische Signalgebung zurückzuführen ist. Mechanische Belastung ist für die ordnungsgemäße Regulierung der Sehnengene von wesentlicher Bedeutung: Lähmung oder Entlastung reduziert wichtige mechanosensitive Transkriptionsfaktoren wie Egr1 und unterbricht die TGF-β-vermittelte Scx-Signalgebung, was die Regenerationsfähigkeit beeinträchtigt. Zugbelastung fördert die sehnenspezifische Genexpression und unterdrückt gleichzeitig Knorpelgene, während Kompression oder Entlastung das Gleichgewicht in Richtung chondrogener oder degenerativer Phänotypen verschiebt. Obwohl Kollagen III gemeinhin mit Narbengewebe in Verbindung gebracht wird, zeigen Evidenzen aus regenerativen Modellen, dass seine frühe Hochregulierung Teil der normalen Reparatur ist. Anhaltende Elevation, insbesondere unter Entlastungsbedingungen, spiegelt eher eine fehlgeschlagene Reifung als die Ursache der Degeneration wider. Selbst eine minimale mechanische ZERRUNG reicht aus, um die Genexpression der Matrix zu regulieren und die mechanische Genesung zu verbessern, was die extreme Sensitiviät der Sehnenzellen gegenüber ihrer Belastungsumgebung verdeutlicht. Zusammengenommen legen diese Ergebnisse nahe, dass sowohl fehlende als auch abweichende mechanische Kräfte die normale Progression von einer frühen Reparaturmatrix zu einer reifen, mechanisch kompetenten Sehne stören.
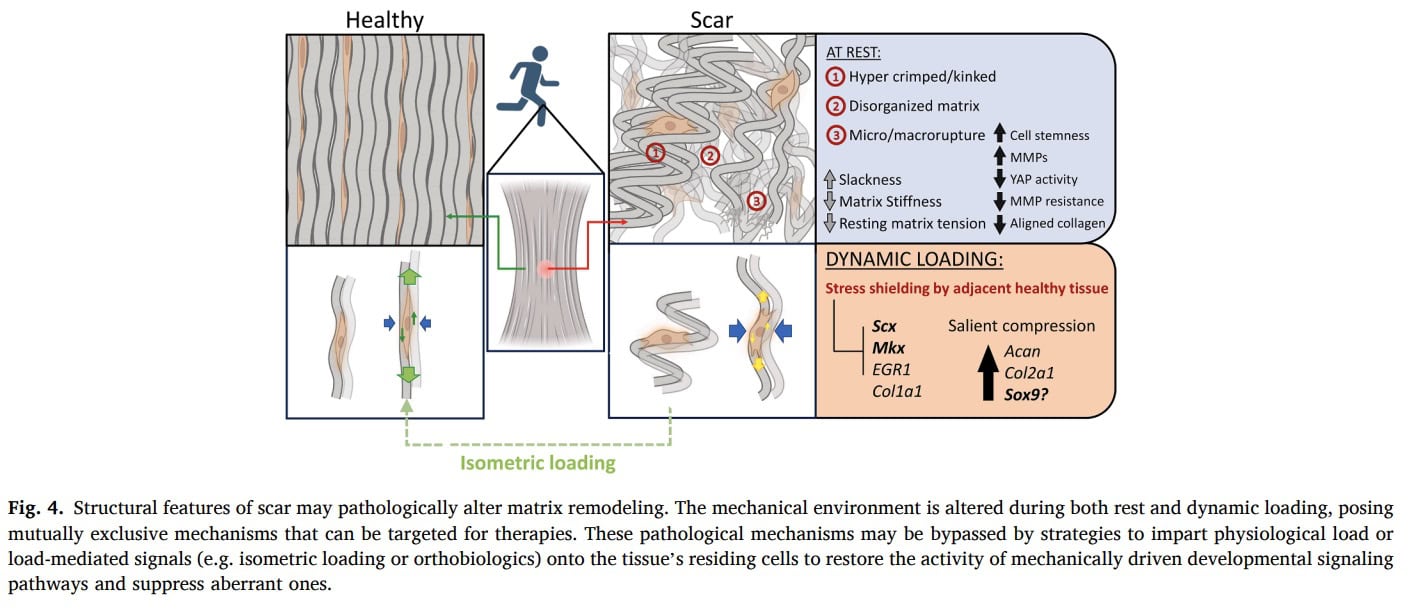
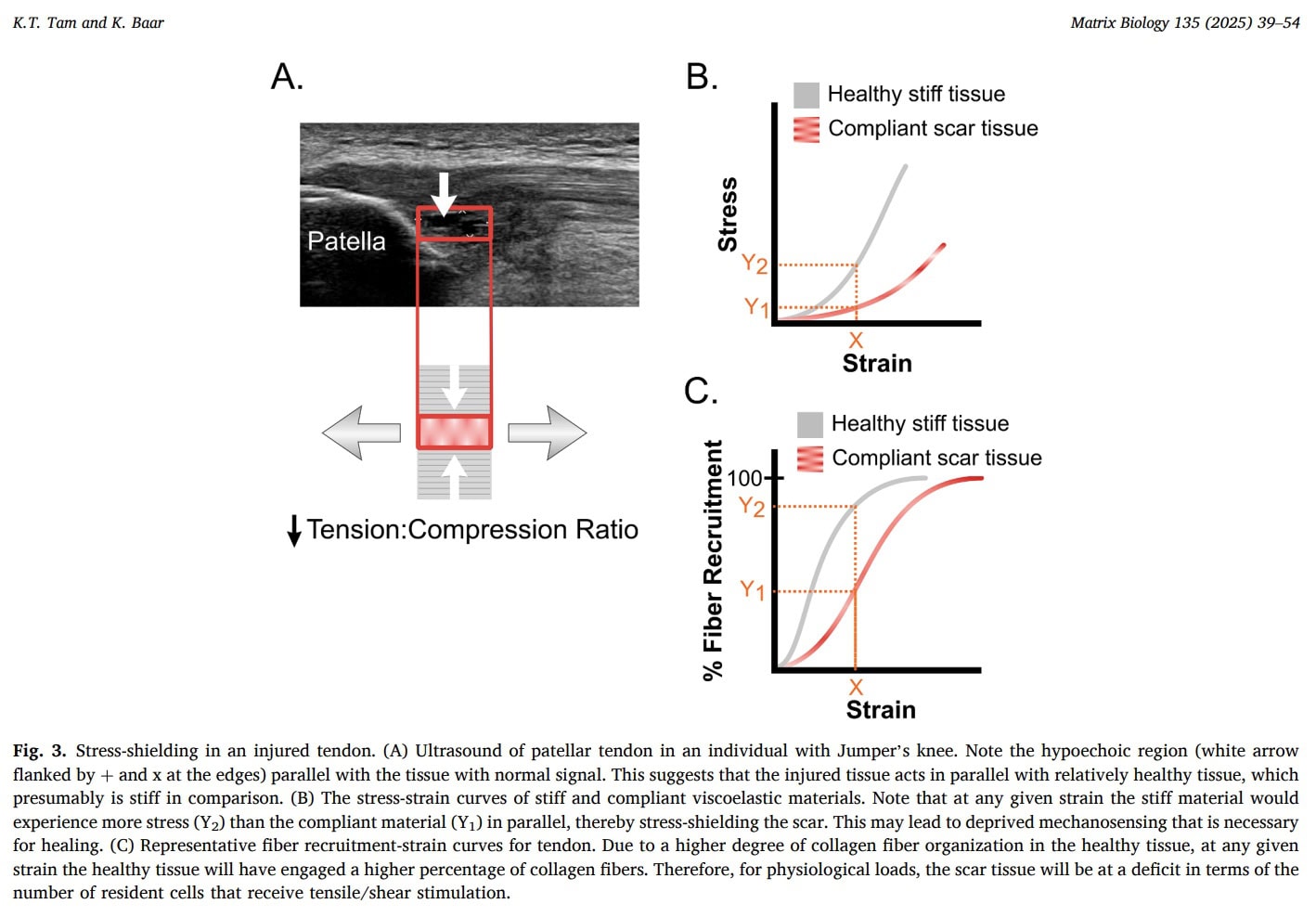
Stress-Abschirmung
Mit der Progression der Tendinopathie können degenerative Sehnenregionen symptomatisch werden und unter Stress stehen. Bei mechanischer Belastung werden steifere und gesündere Teile der Sehne bevorzugt belastet, während die nachgiebigeren degenerativen Bereiche unbelastet bleiben. Dieses biomechanische Phänomen führt zu einer weiteren Verringerung der mechanischen Stimulation des erkrankten Gewebes und kann zu einer Beeinträchtigung der Beanspruchung und der Remodellierung beitragen. Da der degenerative Anteil nur eine geringe effektive Belastung erfährt, ist seine Fähigkeit zur Anpassung der Sehne durch mechanische Belastung vermindert ist.
Sehnen weisen ein viskoelastisches Verhalten auf, das therapeutisch genutzt werden kann. Zwei Schlüsseleigenschaften sind die Stress-Relaxation - die allmähliche Abnahme der inneren Spannung während einer anhaltenden Dehnung - und das Kriechen, die zeitabhängige Verformung von Gewebe unter konstanter Belastung. Diese Eigenschaften legen nahe, dass kontrollierte, anhaltende Belastungsstrategien die mechanische Stimulation degenerativer Regionen trotz Stressabschirmung fördern können.
Isometrische Kontraktionen können eine wertvolle Belastungsmodalität darstellen. Experimentelle Modelle haben gezeigt, dass isometrische Belastung die tenogene Genexpression hochregulieren kann. Verlängerte isometrische Kontraktionen können in gesünderen Sehnenregionen eine Stress-Relaxation auslösen, während sie in degenerativen Bereichen eine Zerrung und mechanische Dehnung zulassen. Dies könnte die Lastübertragung auf das vernarbte Gewebe erleichtern und möglicherweise die biologische und strukturelle Anpassung unterstützen.
Fragen und Gedanken
Tam et al. (2025) gehen davon aus, dass bei Tendinopathie nachgiebiges Narbengewebe parallel zu steiferer gesunder Sehne sitzt und mechanisch "stressabgeschirmt" wird, was bedeutet, dass bei normaler physiologischer ZERRUNG weniger Kollagenfasern und ansässige Zellen innerhalb der Narbe tatsächlich Zugspannung erfahren. Da wichtige tenogene Regulatoren belastungsempfindlich sind, kann eine unzureichende Stress-Übertragung die Narbenreifung verhindern und stattdessen das Anhalten eines unreifen oder fibroknorpelartigen Phänotyps begünstigen. Für die klinische Praxis untermauert dieses Modell den Grundgedanken einer sorgfältig dosierten mechanischen Belastung anstelle einer längeren Entlastung: Es hat sich gezeigt, dass vollständiger Stressentzug die tenogene Genexpression und die mechanische Genesung beeinträchtigt. Die Autoren weisen ferner darauf hin, dass eine anhaltende Belastung, die ein viskoelastisches Kriechen ermöglicht (z. B. isometrische Kontraktionen), dazu beitragen kann, VERSPANNUNGEN in die Narbe zu übertragen und die tenogenen Bahnen zu aktivieren, während eine unangemessene oder fehlende Belastung die Degeneration aufrechterhalten kann. Es ist jedoch wichtig zu betonen, dass dieser mechanobiologische Rahmen zwar eine plausible Erklärung dafür liefert, warum kontrollierte Belastung vorteilhaft sein könnte und warum die Angst vor jeglicher Belastung fehl am Platze ist, dass aber direkte klinische Evidenz dafür, dass spezifische Belastungsstrategien die Stress-Abschirmung beim Menschen "überwinden", in dieser Arbeit noch nicht erbracht wurde.
Isometrische Belastung ist eine vielversprechende Modalität für die Rehabilitation der Sehnen, aber die optimalen Trainingsparameter bleiben ungewiss. In dieser Fallstudiewurde bei einem Athleten mit chronischer Tendinopathie der Patella ein kombiniertes isometrisches Belastungsprogramm und ein Protokoll zur Nahrungsergänzung angewandt. Die Ernährungsstrategie bestand aus 15 g Gelatine mit 225 mg Vitamin C, die etwa eine Stunde vor dem Training eingenommen wurden, um die Synthese von Kollagen zu unterstützen.
Das isometrische Übungsprogramm zielte auf die Belastung der Sehne im mittleren Bereich ab, wobei sowohl offene kettenübungen (Beinstreckung und Beinpresse) als auch geschlossene kettenübungen (spanische Kniebeuge) eingesetzt wurden. Die isometrische Haltezeit betrug anfangs 10 Sekunden und wurde schrittweise in 5-Sekunden-Schritten bis zu einem Maximum von 30 Sekunden erhöht. Das Trainingsvolumen lag zwischen einem und drei Sätzen mit zwei bis vier Wiederholungen bei einer Intensität von mehr als 80 % des monatlich neu berechneten Maximalkraftwerts für eine Wiederholung (1 RM). Die Sitzungen dauerten ca. 10 Minuten, wobei die Haltezeiten auf der Grundlage der Evidenz gewählt wurden, dass die VERSPANNUNGEN der Patellasehne innerhalb von 30 Sekunden nach einer anhaltenden Kontraktion um ca. 60 % abnehmen und danach nur noch geringfügig.
Während der 18-monatigen Intervention wurde eine progressive Erhöhung der Belastung und der Haltedauer mit einer Verbesserung der Kraft bei allen Aufgaben mit Widerstand (Beinstreckung, Beinpresse und spanische Kniebeuge) in Verbindung gebracht. Die Magnetresonanztomographie (MRT) bei Studienbeginn, nach 12 Monaten und nach 18 Monaten zeigte eine Verringerung der Reaktivität der Sehne, einen vergrößerten Sehnendurchmesser an der Mittelsubstanz und eine verringerte Dicke an den proximalen Ansätzen, was auf eine strukturelle Umstrukturierung hindeutet. Der Athlet berichtete über eine progressive Verringerung der Schmerzen und war bei der 18-monatigen Verlaufskontrolle schmerzfrei.
Diese Beobachtungen legen nahe, dass isometrisches Training, insbesondere in Kombination mit Ernährungsstrategien, die die Synthese von Kollagen unterstützen, die Anpassung der Sehne und die Verbesserung der Symptome fördern kann. Die Evidenz bleibt jedoch auf experimentelle Studien und einzelne Fallberichte beschränkt. Größere kontrollierte Studien sind erforderlich, um die Wirksamkeit und die optimalen Parameter isometrischer Protokolle zu bestimmen. Darüber hinaus variieren die Eigenschaften der Sehnen je nach anatomischer Lage, Querschnittsfläche und mechanischer Umgebung, was das viskoelastische Verhalten und die geeigneten Belastungsstrategien beeinflussen kann. Wie in dieser Übersicht betont wird, hängt eine erfolgreiche Rehabilitation wahrscheinlich davon ab, ein angemessenes Gleichgewicht zwischen Unter- und Überbelastung zu erreichen, was den Bedarf an zuverlässigen klinischen Instrumenten zur Überwachung der mechanischen Belastung für die Sehnenanpassung unterstreicht. mechanischen Belastung für die Anpassung der Sehne.
Talk nerdy to me
Obwohl narrative Übersichten mit inhärenten Verzerrungen, wie z. B. Auswahlverzerrungen, behaftet sind, liefert diese Übersicht wichtige biologische Zusammenhänge, die Physiotherapeut/innen dabei helfen können, die Struktur der Sehnen und die Mechanobiologie bei der Behandlung von Tendinopathien besser zu verstehen. Die Kenntnis der genetischen Regulierung, der Transkriptionswege, der Aminosäuredynamik und des Proteinumbaus trägt zu einem tieferen Verständnis der Heilung und Anpassung von Sehnen bei und kann so zu Rehabilitationsstrategien beitragen. Die meisten mechanistischen Evidenzen stammen jedoch aus Tiermodellen, und eine direkte Extrapolation auf die Pathologie menschlicher Sehnen ist nur begrenzt möglich.
Da zur Stärkung der Evidenzbasis fortgeschrittenere klinische Studien erforderlich sind, wird der folgende Artikel dieser Reihe die Daten einer Studie aus dem Jahr 2022 untersuchen, in der ein hochbelastbares Übungsprotokoll zur Vergrößerung des Sehnenquerschnitts und zur Verbesserung von Schmerzen und Funktion bei Patienten mit Achillessehnen-tendinopathie untersucht wurde.
Botschaften zum Mitnehmen
- Sehnen sind lebende, anpassungsfähige Gewebe. Sie reagieren auf mechanische Belastung durch zelluläre Signalübertragung und Umbau der Matrix. Mechanische Reize treiben die strukturelle ANPASSUNG voran - Sehnen sind keine trägen Strukturen.
- Die biomechanische Belastung ist für die Anpassung unerlässlich. Angemessener mechanischer Stress fördert die Gesundheit und den Umbau der Sehnen und unterstützt die funktionelle Genesung und die strukturelle Verbesserung durch mechanische Belastung der Sehnenanpassung.
- Stress-Abschirmung schränkt die Anpassung ein. Degenerativ Sehnenregionen können entlastet werden, wenn gesünderes Gewebe den größten Teil der mechanischen Belastung trägt. Dies reduziert die wirksame mechanische Stimulation und kann die Genesung behindern.
- Rehabilitation muss Stressabschirmung überwinden. Belastungsstrategien sollten darauf abzielen, mechanische Kräfte auf degeneratives Gewebe zu übertragen und gleichzeitig eine übermäßige Zerrung zu vermeiden. Viskoelastische Eigenschaften (Stressrelaxation und Kriechen) bieten eine biomechanische Grundlage für kontrollierte, therapeutische Belastungen.
- Gleichgewichtige Belastung ist der Schlüssel. Sehnen benötigen einen ausreichenden mechanischen Reiz für die Anpassung, sind jedoch anfällig für Unterbelastung (die zu fortgesetztem Nichtgebrauch führt) und Überlastung (die die Symptome verschlimmern kann). Eine individuelle, progressive Belastung ist unerlässlich.
- Klinische Implikationen für die Physiotherapie. Die Rehabilitation sollte sich auf messbare und progressive Belastungsstrategien konzentrieren, die eine mechanische Stimulation des erkrankten Gewebes wiederherstellen und die Anpassungsfähigkeit der Sehne nutzen.
- Die nächsten Schritte. Der nächste Artikel wird diese biomechanischen Prinzipien in klinische Strategien umsetzen, indem er hochbelastbare Übungsprotokolle und praktische Ansätze zur Optimierung der Sehnenanpassung, der Schmerzreduzierung und der funktionellen Genesung bei Tendinopathie bespricht.
Diese Ressource von Physiotutors bietet zusätzliche Einblicke in die Biologie und Mechanobiologie der Sehnen und bietet klinisch relevante Einblicke in die Funktion und Anpassung der Sehnen.
Referenz
DIE ROLLE DER VMO & QUADS IN DER PFP
Sehen Sie sich diesen KOSTENLOSEN ZWEITEILIGEN VIDEO-VORTRAG der Knieschmerzexpertin Claire Robertson an, die die Literatur zu diesem Thema und ihre Auswirkungen auf die klinische Praxis analysiert.