Влияние механической нагрузки на адаптацию сухожилий - биологические предпосылки для точных вмешательств в физиотерапию
Введение
Несмотря на прогресс в понимании патогенеза тендинопатии, результаты после традиционных консервативных и медикаментозных вмешательств остаются противоречивыми, а многие пациенты испытывают постоянную боль и функциональные ограничения. Широко цитируемая модель континуума, предложенная Джилл Кук, предполагает, что дегенеративная часть сухожилия является структурно необратимой. Однако появляющиеся структурные и механобиологические данные ставят под сомнение это предположение, указывая на то, что ткань сухожилия может сохранять большую способность к адаптации и ремоделированию, чем считалось ранее.
В данном обзоре рассматривается влияние механической нагрузки на адаптацию сухожилия и биологические механизмы, лежащие в основе дегенерации, с особым акцентом на клеточную сигнализацию, ремоделирование матрицы и пути механотрансдукции. Интегрируя последние экспериментальные данные, он призван обеспечить биологически обоснованную базу для назначения упражнений при лечении тендинопатии. Этот теоретический синтез послужит основой для предстоящего обзора, в котором будут рассмотрены стратегии выполнения упражнений с высокой нагрузкой и представлен новый протокол нагрузки при тендинопатии для клинического применения.
Методы
В данном описательном обзоре обобщены результаты многочисленных экспериментальных исследований, проведенных преимущественно на животных моделях.
Результаты
Биологические основы строения сухожилий
Коллаген I типа (COL1/Col1a1) является основным структурным белком тканей сухожилий и связок, обеспечивающим прочность на разрыв. После травмы синтез коллагена увеличивается, однако отложение матрикса во время пролиферативной фазы часто бывает дезорганизованным. В то время как в здоровых сухожилиях коллагеновые фибриллы выровнены параллельно механическим силам, в патологических сухожилиях фибриллы меньше, менее сшиты и дезорганизованы. Хотя коллаген I типа обеспечивает более высокую механическую прочность по сравнению с коллагеном III типа, заживающие сухожилия часто содержат большую долю коллагена III типа. Матриксные металлопротеиназы (ММП), ферменты, ответственные за деградацию коллагена, одновременно активны во время ремоделирования тканей.
Поврежденные сухожилия взрослых обычно становятся высококлеточными и развивают дезорганизованный коллагеновый матрикс, характеризующийся фибриллами малого диаметра, что приводит к дегенеративному фенотипу ткани.
Регенерация тканей и рекапитуляция развития
В ответ на травму гены, обычно активные во время эмбрионального развития, вновь экспрессируются. Популяции стволовых и пролиферативных клеток расширяются и дифференцируются в специализированные ткани, однако сухожилия взрослых людей, как правило, не могут полностью регенерировать, часто оставляя остаточный дегенеративный матрикс. Напротив, неонатальные модели демонстрируют большую способность к функциональному восстановлению, а организация тканей напоминает процессы развития. Эти данные свидетельствуют о том, что способность к регенерации может зависеть от способности к рекапитуляции программ развития, что проявляется в более молодых организмах и некоторых экспериментальных моделях в большей степени, чем при заживлении сухожилий взрослого человека.
Свойства материалов отражают механические требования
Сухожилия можно классифицировать в соответствии с их механической функцией как энергоаккумулирующие или позиционные структуры. Энергоаккумулирующие сухожилия, такие как ахиллово сухожилие, поглощают и отдают механическую энергию для повышения эффективности локомоции. Позиционные сухожилия, примером которых может служить переднее большеберцовое сухожилие, в первую очередь позиционируют суставы и облегчают такие движения, как освобождение стопы при ходьбе. Эти функциональные различия отражаются в структурных свойствах: сухожилия, накапливающие энергию, обычно имеют большую площадь поперечного сечения, компенсируя меньшую жесткость материала для обеспечения упругого накопления энергии. Сухожилия в пределах одной кинетической цепи также могут иметь различные механические характеристики. Например, сухожилие четырехглавой мышцы и сухожилие надколенника действуют последовательно, но демонстрируют разные жесткостные свойства, причем сухожилие четырехглавой мышцы примерно в два раза менее жесткое. Это различие, вероятно, отражает их механическую среду - костно-костное введение сухожилия надколенника и мышечно-костное прикрепление сухожилия четырехглавой мышцы, - которая накладывает различные модели нагрузки и, следовательно, влияет на механическая нагрузка на адаптацию сухожилия и требования к материалам.
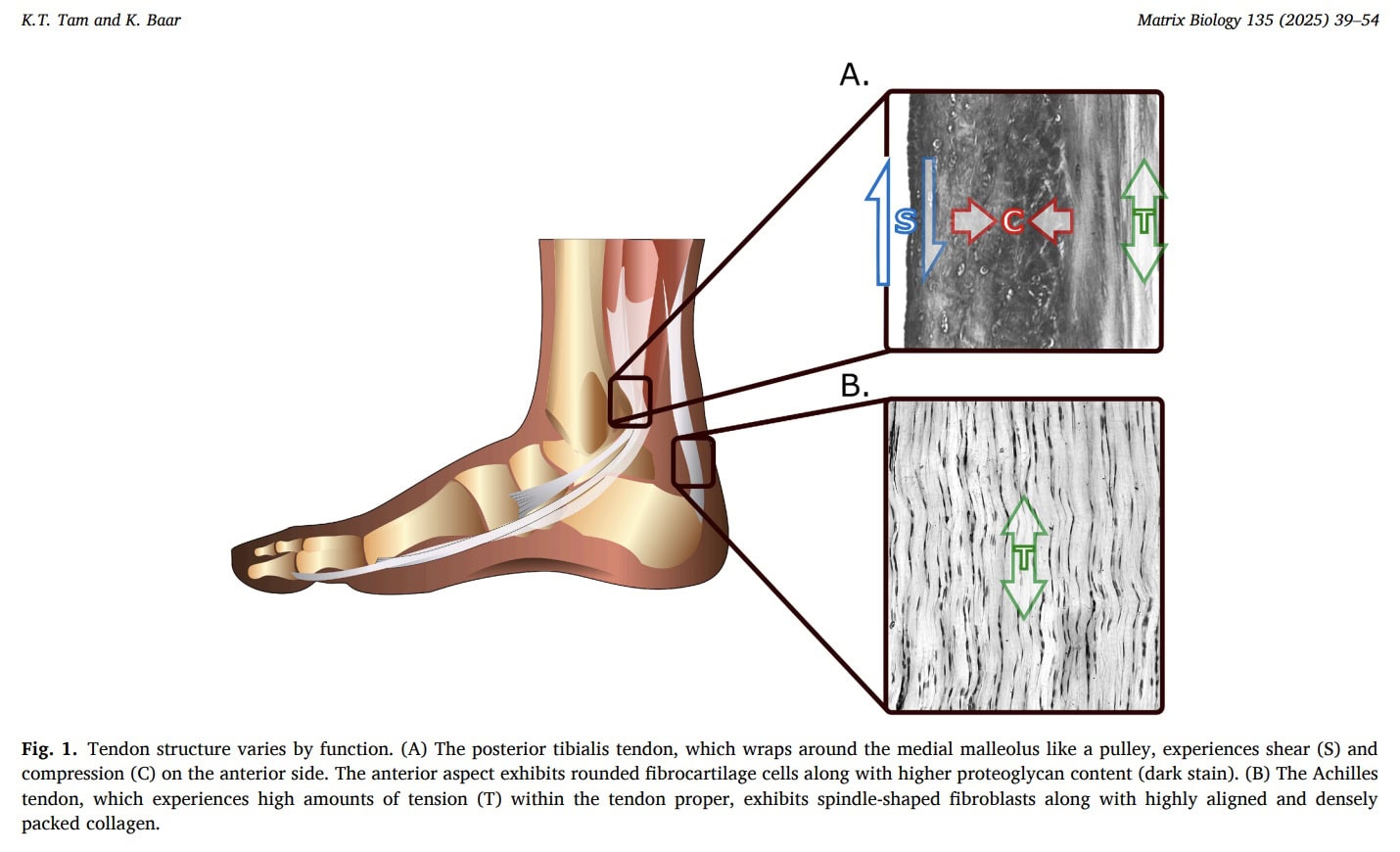
Компрессия
Сжимающие силы часто действуют на сухожилия, особенно там, где они обхватывают костные или ретинальные структуры. Экспериментальные исследования на животных моделях показывают, что снятие сжимающей нагрузки уменьшает жесткость сухожилия и изменяет структурную адаптацию, что указывает на то, что сухожилия, подвергающиеся сжатию, ремоделируются, чтобы приспособиться к этой механической среде. У людей сжатые участки сухожилий часто демонстрируют фиброкартилагиновые особенности, богатые коллагеном II типа, специализированные для сопротивления сжимающим силам.
Shear
Силы сдвига возникают в результате относительного скольжения между сухожилиями, связками, мышцами и прилегающими тканями. В ахилловом сухожилии дифференциальное скольжение между пучками способствует передаче силы, но с возрастом может уменьшаться, что потенциально способствует уменьшению диапазона движения и нарушению распределения силы. Снижение скользящей способности может частично объяснить более высокую частоту разрывов ахиллова сухожилия у пожилых людей. Как и в случае адаптации к сжатию, снижение механической нагрузки может способствовать дегенеративным изменениям, повышению риска травм и дезадаптации.
Специфические силы управляют специфическими молекулярными программами
Судьба клеток и состав ткани сильно зависят от механической среды через пути механотрансдукции, что подчеркивает важность механической нагрузки на адаптацию сухожилия. Механические силы инициируют биологические и метаболические адаптации, которые регулируют структуру и функцию ткани, хотя конкретные пути, регулирующие заживление сухожилий, остаются не до конца понятными. В последующих разделах рассматриваются биомеханические эффекты различных видов нагрузки на адаптацию и восстановление сухожилий.
Напряжение
Манипулирование механической средой, включая механическая нагрузкаиграет центральную роль в ремоделировании сухожилий и их функциональной адаптации. Растягивающая нагрузка способствует ремоделированию тканей, но баланс между полезными и потенциально вредными нагрузками остается критическим. Более глубокое биомеханическое понимание стратегий нагрузки необходимо для оптимизации реабилитации и адаптации сухожилий.
Склераксис (Scx) - ключевой транскрипционный фактор, участвующий в развитии сухожилий и регуляции коллагена. Во время эмбриогенеза Scx способствует синтезу коллагена I типа (COL1), связываясь с регуляторными участками гена Col1a1. На его экспрессию влияют мышечная активность и механическая нагрузка. Однако во взрослых сухожилиях Scx, по-видимому, менее важен для адаптивного роста. Несколько теногенных генов, включая Col1a1, теномодулин (Tnmd), фибромодулин (Fmod) и Mohawk (Mkx), могут быть повышены в ответ на нагрузку без соответствующих изменений в экспрессии Scx. Это позволяет предположить, что адаптация сухожилия может происходить независимо от Scx и что его основная роль может быть связана с ранним формированием фибрилл, а не с последующим ростом фибрилл. Напротив, Mkx, по-видимому, способствует увеличению и созреванию фибрилл в ответ на механическую стимуляцию, поддерживая свою роль в структурной адаптации сухожилия.
Заживающие сухожилия взрослых людей часто демонстрируют черты, напоминающие ткани развития, включая коллагеновые фибриллы малого диаметра и повышенную экспрессию Scx. Однако, в отличие от эмбрионального развития, заживающий матрикс часто не успевает созреть в организованную, несущую нагрузку ткань. Одно из объяснений заключается в том, что механические сигналы не могут адекватно передаваться через рубцовый матрикс - явление, соответствующее экранированию стресса (подробнее об этом ниже). Нарушение механической сигнализации может снижать активацию механочувствительных путей, таких как Mkx, ограничивая созревание коллагеновых фибрилл и способствуя формированию механически неполноценной рубцовой ткани.
Компрессия
Сжимающие силы регулируют дифференцировку сухожильных клеток и состав матрикса. В областях, подвергающихся компрессии, таких как энтезис и сухожильные тяжи, обычно развиваются фиброзно-хрящевые черты, характеризующиеся экспрессией маркеров хряща, включая Col2a1 и аггрекан. В процессе развития прогениторы сухожилий первоначально совместно экспрессируют Scx и Sox9 (хондрогенный транскрипционный фактор), а затем разделяются на адаптированные к растяжению сухожильные клетки и адаптированные к сжатию фиброхрящевые клетки. Экспериментальные данные показывают, что длительное сжатие может вызывать формирование хрящеподобной ткани в сухожилии, в то время как растяжение способствует экспрессии генов, специфичных для сухожилия, и подавляет хондрогенные пути. В отсутствие Mkx растяжение может парадоксальным образом способствовать экспрессии хондрогенных генов, что приводит к эктопическому формированию фиброхряща. Полученные данные свидетельствуют о том, что клетки сухожилий обладают мультипотентным потенциалом и что механическая нагрузка регулирует дифференцировку через транскрипционные программы, чувствительные к растяжению и сжатию.
Стрижка
Лубрицин и гиалуроновая кислота являются важными посредниками скольжения сухожильных пучков и сопротивления сдвигу. Однако их биологическая регуляция и реакция на механическую нагрузку остаются недостаточно охарактеризованными, что ограничивает понимание их роли в патологии сухожилий и адаптации.
Пространственное расположение
Организация коллагена необходима для функционирования сухожилия и в значительной степени регулируется механическим напряжением. Во время развития растягивающие силы выравнивают клетки и коллагеновые фибриллы с помощью специализированных структур (фибрипозиторов), создавая параллельную архитектуру, характерную для здоровых сухожилий. Даже в ацеллюлярных коллагеновых матрицах растяжение может увеличить выравнивание и плотность фибрилл, и эти изменения могут сохраняться после разгрузки. Однако постоянство ремоделирования зависит от сшивки матрикса, которая может снижать адаптивность при старении или метаболических изменениях в тканях, например, при диабете. Растягивающая нагрузка также повышает устойчивость к деградации коллагена и активирует биохимические пути (включая Mkx), которые поддерживают созревание фибрилл. Адаптация сухожилий, таким образом, отражает взаимодействие пассивного механического выравнивания и активной клеточной сигнализации в ответ на механическую нагрузкупроцесс, который регулирует структурное ремоделирование и функциональную оптимизацию.
Отсутствующие и аберрантные силы играют роль в дегенерации сухожилий и связок
Заживающие сухожилия часто напоминают незрелые или эмбриональные ткани, демонстрируя повышенную экспрессию Scx, увеличенное количество фибриллогенных коллагенов (III, V, XI), коллагеновые фибриллы малого диаметра, высокую клеточность, васкуляризацию и присутствие Scx+/Sox9+ прогениторов. Эти особенности позволяют предположить, что травмированное сухожилие восстанавливает программу развития, но не может продвинуться к полному механическому созреванию, вероятно, из-за изменения механической сигнализации. Механическая нагрузка необходима для правильной регуляции генов сухожилия: паралич или разгрузка снижают уровень ключевых механочувствительных факторов транскрипции, таких как Egr1, и нарушают TGF-β-опосредованную сигнализацию Scx, ухудшая регенеративную способность. Растягивающая нагрузка способствует экспрессии специфических для сухожилия генов, подавляя при этом гены хряща, в то время как сжатие или разгрузка смещают баланс в сторону хондрогенных или дегенеративных фенотипов. Хотя коллаген III обычно ассоциируется с рубцовой тканью, данные регенеративных моделей показывают, что его ранняя регуляция является частью нормального восстановления. Постоянное повышение, особенно в условиях разгрузки, отражает неудачное созревание, а не причину дегенерации. Даже минимальная механическая нагрузка достаточна для регуляции экспрессии генов матрикса и улучшения механического восстановления, что подчеркивает чрезвычайную чувствительность клеток сухожилия к условиям нагрузки. В совокупности эти данные свидетельствуют о том, что как отсутствие, так и аберрантные механические силы нарушают нормальный процесс перехода от раннего восстановительного матрикса к зрелому, механически компетентному сухожилию.
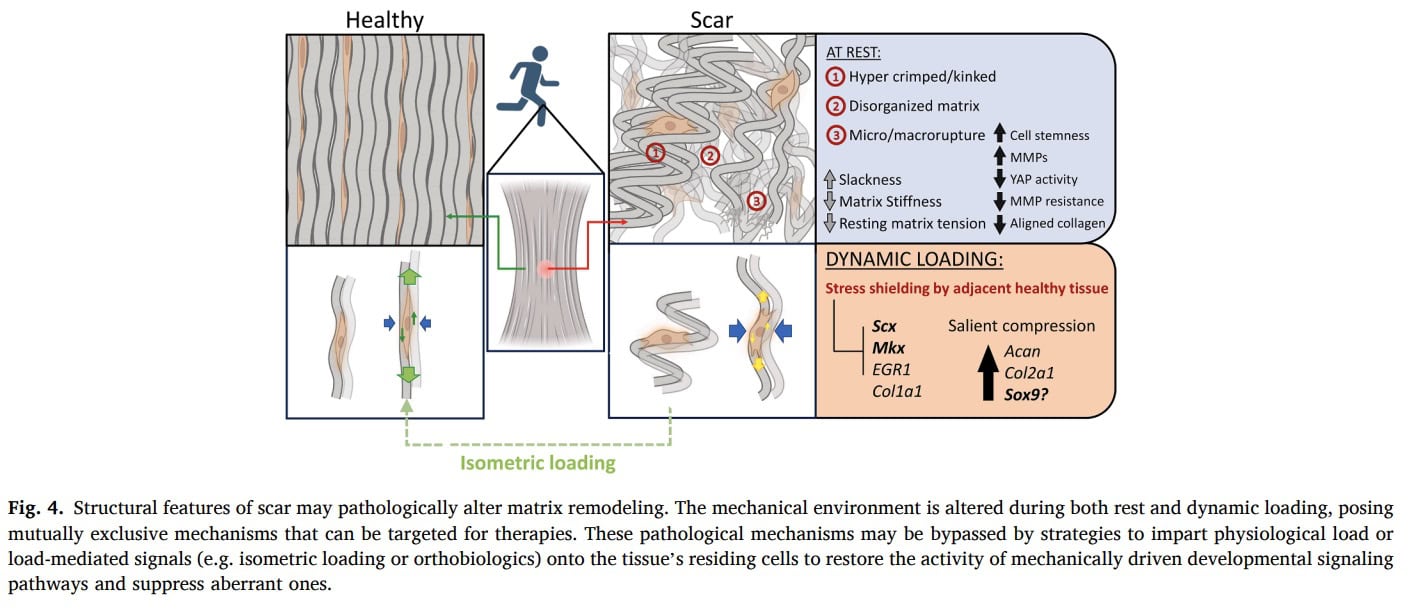
Защита от стресса
По мере прогрессирования тендинопатии дегенеративные участки сухожилий могут стать симптоматичными и подвергаться стрессовому экранированию. При приложении механической нагрузки более жесткие и здоровые участки сухожилия преимущественно выдерживают нагрузку, в то время как более податливые дегенеративные участки разгружаются. Это биомеханическое явление еще больше снижает механическую стимуляцию больной ткани и может способствовать прекращению использования и ухудшению ремоделирования. Поскольку дегенеративная часть получает мало эффективной нагрузки, ее способность к адаптации сухожилия посредством механической нагрузки уменьшается.
Сухожилия демонстрируют вязкоупругое поведение, которое может быть использовано в терапевтических целях. Два ключевых свойства: релаксация напряжения - постепенное снижение внутреннего напряжения при длительном растяжении - и ползучесть - зависящая от времени деформация ткани при постоянном напряжении. Эти свойства позволяют предположить, что стратегии контролируемой, продолжительной нагрузки могут способствовать механической стимуляции дегенеративных областей, несмотря на экранирование стресса.
Изометрические сокращения могут представлять собой ценный способ нагрузки. Экспериментальные модели показали, что изометрическая нагрузка может стимулировать экспрессию теногенных генов. Длительные изометрические сокращения могут вызывать релаксацию напряжения в более здоровых участках сухожилия, одновременно допуская ползучесть и механическую деформацию в дегенеративных участках. Это может способствовать передаче нагрузки на рубцовую ткань и потенциально поддерживать биологическую и структурную адаптацию.
Вопросы и мысли
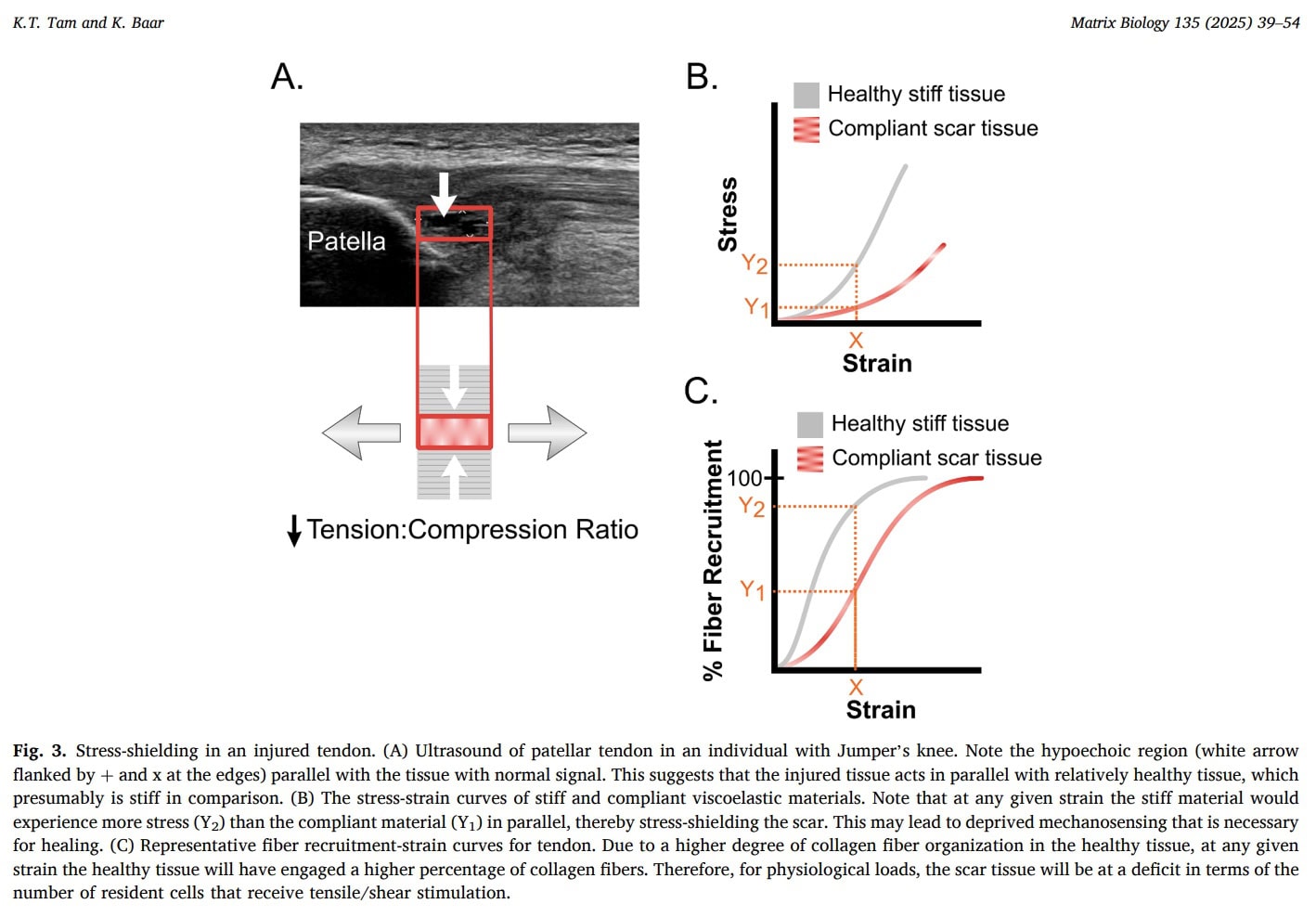
Там и др. (2025) предполагают, что при тендинопатии податливая рубцовая ткань может располагаться параллельно более жесткому здоровому сухожилию и становится механически "защищенной от стресса", что означает, что при нормальных физиологических уровнях деформации меньшее количество коллагеновых волокон и резидентных клеток внутри рубца фактически испытывают растягивающее напряжение. Поскольку ключевые теногенные регуляторы чувствительны к нагрузке, недостаточная передача стресса может препятствовать созреванию рубца и вместо этого способствовать сохранению незрелого или фиброхрящеподобного фенотипа. Для клинической практики эта модель поддерживает обоснование необходимости тщательно дозированной механической нагрузки, а не длительной разгрузки: было показано, что полная депривация стресса ухудшает экспрессию теногенных генов и механическое восстановление. Авторы также предполагают, что длительная нагрузка, обеспечивающая вязкоупругую ползучесть (например, изометрические сокращения), может способствовать передаче напряжения в рубец и активации теногенных путей, в то время как неправильная нагрузка или ее отсутствие могут способствовать дегенерации. Однако важно подчеркнуть, что, хотя эта механобиологическая схема дает правдоподобное объяснение тому, почему контролируемая нагрузка может быть полезной и почему страх перед любой нагрузкой может быть неуместным, прямых клинических доказательств того, что конкретные стратегии нагрузки "преодолевают" стресс-экранирование у людей, в рамках данной работы пока не получено.
Изометрическая нагрузка является перспективным методом реабилитации сухожилий, однако оптимальные параметры тренировок остаются неясными. В данном исследованииспортсмена с хронической тендинопатией надколенника была применена комбинированная программа изометрической нагрузки и протокол диетического питания. Диетическая стратегия состояла из 15 г желатина с 225 мг витамина С, употребляемых примерно за час до тренировки с целью поддержания синтеза коллагена.
Программа изометрических упражнений была направлена на среднюю нагрузку на сухожилие с использованием как упражнений с открытой цепью (разгибание ног и жим ногами), так и с закрытой цепью (испанские приседания). Продолжительность изометрического удержания вначале составляла 10 секунд и постепенно увеличивалась с шагом в 5 секунд до максимального значения в 30 секунд. Тренировочный объем варьировался от одного до трех сетов из двух-четырех повторений, выполняемых с интенсивностью, превышающей 80 % от максимальной нагрузки в одном повторении (1 RM), которая пересчитывалась ежемесячно. Сеансы длились около 10 минут, а продолжительность удержания была выбрана на основе данных, свидетельствующих о том, что напряжение сухожилия надколенника снижается примерно на 60 % в течение 30 секунд после устойчивого сокращения и лишь незначительно в последующем.
В течение 18 месяцев постепенное увеличение нагрузки и продолжительности удержания было связано с улучшением силы во всех заданиях с сопротивлением (разгибание ног, жим ногами и удержание испанских приседаний). Магнитно-резонансная томография (МРТ) на исходном уровне, через 12 месяцев и 18 месяцев показала снижение реактивности сухожилий, увеличение диаметра сухожилий в средней части и уменьшение толщины в проксимальном отделе, что соответствует структурному ремоделированию. Спортсмен сообщил о прогрессирующем уменьшении боли и был свободен от боли на 18-м месяце наблюдения.
Эти наблюдения позволяют предположить, что изометрические тренировки, особенно в сочетании со стратегиями питания, поддерживающими синтез коллагена, могут способствовать адаптации сухожилий и улучшению симптомов. Однако доказательная база по-прежнему ограничивается экспериментальными исследованиями и единичными случаями. Для определения эффективности и оптимальных параметров изометрических протоколов необходимы более крупные контролируемые исследования. Кроме того, свойства сухожилий зависят от анатомического расположения, площади поперечного сечения и механической среды, что может влиять на вязкоупругое поведение и соответствующие стратегии нагрузки. Как подчеркивается в данном обзоре, успешная реабилитация, вероятно, зависит от достижения соответствующего баланса между недостаточной и чрезмерной нагрузкой, что подчеркивает необходимость надежных клинических инструментов для мониторинга механической нагрузки для адаптации сухожилий. механической нагрузки для адаптации сухожилий.
Поговори со мной о ботанике
Несмотря на то, что повествовательные обзоры подвержены присущей им необъективности, такой как предвзятость отбора, данный обзор обеспечивает важный биологический контекст, который может помочь физиотерапевтам лучше понять структуру сухожилий и механобиологию при лечении тендинопатии. Знания о генетической регуляции, транскрипционных путях, динамике аминокислот и ремоделировании белков способствуют более глубокому пониманию процессов заживления и адаптации сухожилий, что может стать основой для разработки стратегий реабилитации. Однако большинство механистических данных получено на животных моделях, и прямая экстраполяция на патологию сухожилий человека остается ограниченной.
Хотя для укрепления доказательной базы необходимы более сложные клинические испытания, в следующей статье этой серии будут рассмотрены данные исследования 2022 года, в котором изучался протокол упражнений с высокой нагрузкой, направленный на увеличение площади поперечного сечения сухожилия и улучшение боли и функции у пациентов с ахилловой тендинопатией.
Напутствия на будущее
- Сухожилия - это живые, адаптивные ткани. Они реагируют на механическую нагрузку посредством клеточной сигнализации и ремоделирования матрицы. Механические стимулы приводят к структурной адаптации - сухожилия не являются инертными структурами.
- Биомеханическая нагрузка необходима для адаптации. Соответствующее механическое напряжение способствует здоровью и ремоделированию сухожилий, поддерживая функциональное восстановление и улучшение структуры за счет механической нагрузки на адаптацию сухожилий.
- Экранирование стресса ограничивает адаптацию. Дегенеративные участки сухожилий могут быть разгружены, когда большую часть механической нагрузки несут здоровые ткани. Это снижает эффективность механической стимуляции и может препятствовать восстановлению.
- Реабилитация должна преодолеть экранирование напряжения. Стратегии нагрузки должны быть направлены на передачу механических усилий дегенеративным тканям, избегая при этом чрезмерной деформации. Вязкоупругие свойства (релаксация напряжения и ползучесть) обеспечивают биомеханическую основу для контролируемой, терапевтической нагрузки.
- Сбалансированная нагрузка - ключевой момент. Сухожилиям требуется достаточный механический стимул для адаптации, но они уязвимы к недогрузке (которая закрепляет отказ от использования) и перегрузке (которая может усугубить симптомы). Индивидуальная прогрессивная нагрузка имеет большое значение.
- Клинические последствия для физиотерапии. Реабилитация должна быть сосредоточена на измеримых и прогрессивных стратегиях нагрузки, которые восстанавливают механическую стимуляцию больной ткани и используют адаптивность сухожилий.
- Следующие шаги. В предстоящей статье эти биомеханические принципы будут воплощены в клинические стратегии, будут рассмотрены протоколы упражнений с высокой нагрузкой и практические подходы к оптимизации адаптации сухожилий, уменьшению боли и функциональному восстановлению при тендинопатии.
Этот ресурс Physiotutors предоставляет дополнительные перспективы биологии сухожилий и механобиологии, предлагая клинически значимые взгляды на функцию сухожилий и адаптацию.
Ссылка
РОЛЬ ВМО И КВАДОВ В ПФП
Смотри БЕСПЛАТНАЯ ВИДЕОЛЕКЦИЯ ИЗ ДВУХ ЧАСТЕЙ Эксперт по боли в коленях Клэр Робертсон который анализирует литературу по этой теме и то, как она Влияет на клиническую практику.