Efecto de la carga mecánica en la adaptación del tendón: base biológica para intervenciones de fisioterapia precisas
Introducción
A pesar de los avances en nuestra comprensión de la patogénesis de la tendinopatía, los resultados tras las intervenciones conservadoras y médicas tradicionales siguen siendo inconsistentes, y muchos pacientes experimentan dolor persistente y limitaciones funcionales. El ampliamente citado modelo continuo propuesto por Jill Cook sugiere que la porción degenerativa de un tendón es estructuralmente irreversible. Sin embargo, las evidencias estructurales y mecanobiológicas emergentes desafían esta suposición, indicando que el tejido del tendón puede retener una mayor capacidad de adaptación y remodelación de lo que se pensaba anteriormente.
Esta revisión explora la influencia de la carga mecánica en la adaptación del tendón y los mecanismos biológicos subyacentes a la degeneración, con especial atención a la señalización celular, la remodelación de la matriz y las vías de mecanotransducción. Mediante la integración de hallazgos experimentales recientes, se pretende proporcionar un marco biológicamente fundamentado para informar sobre la prescripción de ejercicio en el tratamiento de la tendinopatía. Esta síntesis teórica sirve de base para una próxima revisión en la que se examinarán estrategias de ejercicio con cargas elevadas y se introducirá un novedoso protocolo de carga de tendinopatías para su aplicación clínica.
Métodos
Esta revisión narrativa sintetiza los hallazgos de múltiples estudios experimentales, realizados predominantemente en modelos animales.
Resultados
Bases biológicas de la estructura del tendón
El colágeno de tipo I (COL1/Col1a1) es la principal proteína estructural del tejido de tendones y ligamentos, y confiere resistencia a la tracción. Tras una lesión, aumenta la síntesis de colágeno; sin embargo, la deposición de matriz durante la fase proliferativa suele ser desorganizada. Mientras que los tendones sanos presentan fibrillas de colágeno alineadas en paralelo a las fuerzas mecánicas, los tendones patológicos contienen fibrillas más pequeñas, menos reticuladas y desorganizadas. Aunque el colágeno de tipo I proporciona una resistencia mecánica superior a la del colágeno de tipo III, los tendones en cicatrización suelen contener una mayor proporción de colágeno de tipo III. Las metaloproteinasas de la matriz (MMP), enzimas responsables de la degradación del colágeno, están simultáneamente activas durante la remodelación de los tejidos.
Los tendones adultos lesionados suelen volverse muy celulares y desarrollar una matriz de colágeno desorganizada caracterizada por fibrillas de pequeño diámetro, lo que da lugar a un fenotipo de tejido degenerativo.
Regeneración de tejidos y recapitulación del desarrollo
En respuesta a una lesión, los genes normalmente activos durante el desarrollo embrionario vuelven a expresarse. Las poblaciones de células madre y proliferativas se expanden y diferencian en tejidos especializados; sin embargo, los tendones adultos no suelen regenerarse completamente, dejando a menudo una matriz degenerativa residual. Por el contrario, los modelos neonatales demuestran una mayor capacidad de reparación funcional, con una organización de los tejidos que se asemeja a los procesos de desarrollo. Estos hallazgos sugieren que la capacidad regenerativa puede depender de la capacidad de recapitular programas de desarrollo, una característica que parece más robusta en organismos más jóvenes y en ciertos modelos experimentales que en la cicatrización del tendón humano adulto.
Las propiedades de los materiales reflejan las exigencias mecánicas
Los tendones pueden clasificarse según su función mecánica como estructuras de almacenamiento de energía o de posición. Los tendones que almacenan energía, como el Tendón de Aquiles, absorben y devuelven energía mecánica para mejorar la eficiencia locomotora. Los tendones posicionales, ejemplificados por el tendón tibial anterior, principalmente posicionan las articulaciones y facilitan movimientos como el despeje del pie durante la marcha. Estas diferencias funcionales se reflejan en las propiedades estructurales: los tendones que almacenan energía suelen tener una mayor sección transversal, lo que compensa la menor rigidez del material para permitir el almacenamiento elástico de energía. Los tendones de una misma cadena cinética también pueden presentar características mecánicas diferentes. Por ejemplo, el tendón del cuádriceps y el tendón rotuliano funcionan en serie pero presentan propiedades de rigidez distintas, siendo el tendón del cuádriceps aproximadamente dos veces menos rígido. Es probable que esta diferencia refleje sus entornos mecánicos: la inserción hueso-hueso del tendón rotuliano frente a la inserción músculo-hueso del tendón del cuádriceps, que imponen distintos patrones de carga y, por lo tanto, influyen en la carga mecánica sobre la adaptación del tendón y en los requisitos de material. la carga mecánica en la adaptación del tendón y los requisitos de material.
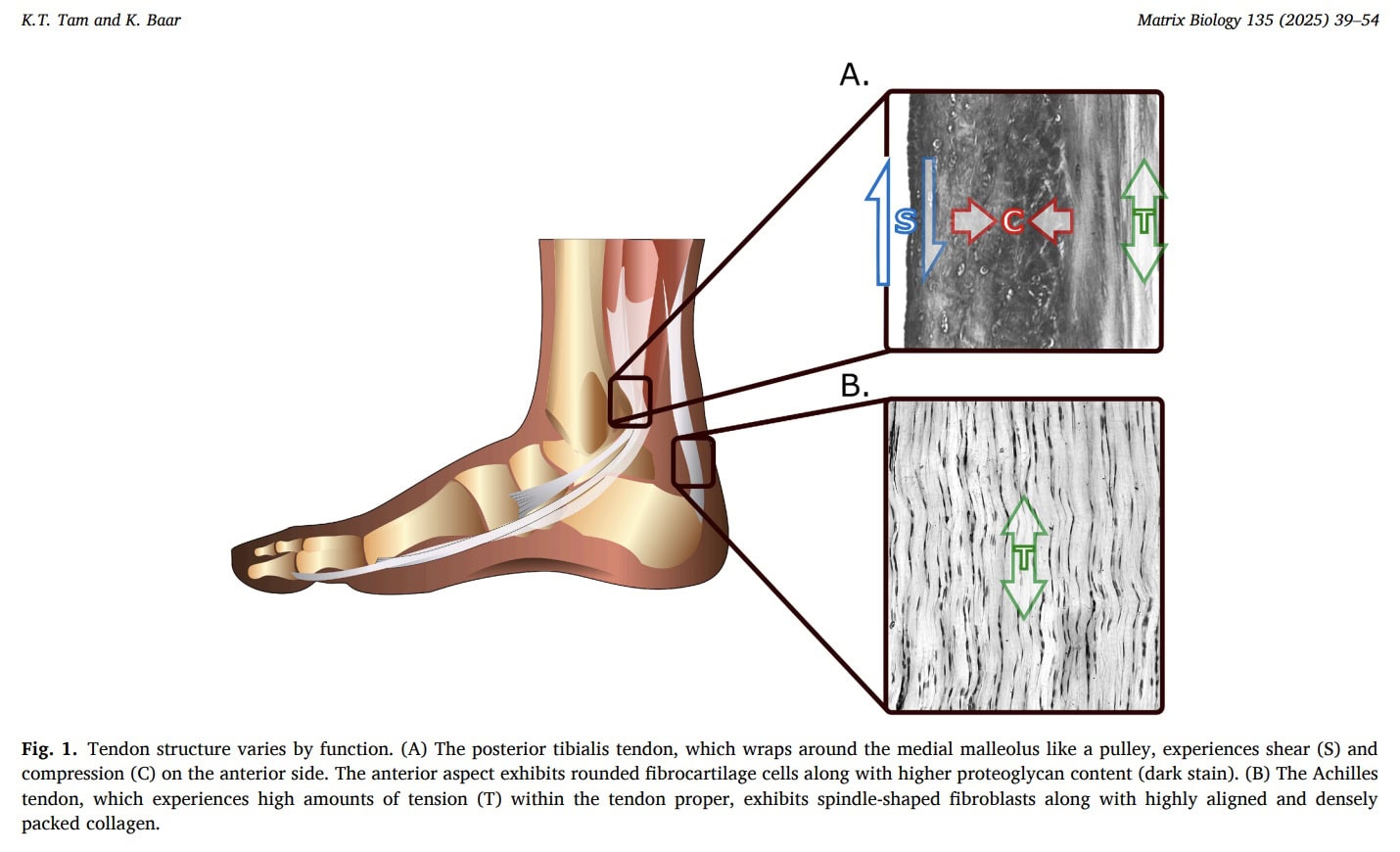
Compresión
Las fuerzas de compresión actúan con frecuencia sobre los tendones, especialmente cuando envuelven estructuras óseas o retinaculares. Estudios experimentales en modelos animales demuestran que la eliminación de la carga compresiva reduce la rigidez del tendón y altera la adaptación estructural, lo que indica que los tendones expuestos a la compresión se remodelan para adaptarse a este entorno mecánico. En los seres humanos, las regiones tendinosas comprimidas suelen presentar características fibrocartilaginosas ricas en colágeno de tipo II, especializadas en la resistencia a las fuerzas de compresión.
Shear
Las fuerzas de cizallamiento surgen del deslizamiento relativo entre tendones, ligamentos, músculos y tejidos adyacentes. En el tendón de Aquiles, el deslizamiento diferencial entre fascículos facilita la transmisión de la fuerza, pero puede disminuir con la edad, lo que puede contribuir a reducir la amplitud de movimiento y a alterar la distribución de la fuerza. Esta disminución de la capacidad de deslizamiento puede explicar en parte la mayor incidencia de rotura del Tendón de Aquiles en personas mayores. Al igual que en la adaptación a la compresión, la reducción de la carga mecánica puede contribuir a los cambios degenerativos, al aumento del riesgo de lesión y a la desadaptación.
Fuerzas específicas impulsan programas moleculares específicos
El destino de las células y la composición de los tejidos están fuertemente influenciados por el entorno mecánico a través de las vías de mecanotransducción, lo que pone de relieve la importancia de la la carga mecánica en la adaptación del tendón. Las fuerzas mecánicas inician adaptaciones biológicas y metabólicas que regulan la estructura y función de los tejidos, aunque las vías específicas que rigen la cicatrización del tendón siguen sin conocerse del todo. En las secciones siguientes se examinan los efectos biomecánicos de las distintas modalidades de carga en la adaptación y reparación del tendón.
Tensión
Manipulación del entorno mecánico, incluida la carga mecánicaes fundamental para la remodelación del tendón y la adaptación funcional. La carga de tracción impulsa la remodelación de los tejidos, pero el equilibrio entre las cargas beneficiosas y las potencialmente perjudiciales sigue siendo crítico. Por lo tanto, para optimizar la rehabilitación y la adaptación del tendón es esencial una mayor comprensión biomecánica de las estrategias de carga.
Scleraxis (Scx) es un factor de transcripción clave implicado en el desarrollo del tendón y la regulación del colágeno. Durante la embriogénesis, Scx promueve la síntesis de colágeno de tipo I (COL1) uniéndose a regiones reguladoras del gen Col1a1. Su expresión se ve influida por la activación muscular y la carga mecánica. Sin embargo, en los tendones adultos, Scx parece menos esencial para el crecimiento adaptativo. Varios genes tenogénicos -incluidos Col1a1, tenomodulina (Tnmd), fibromodulina (Fmod) y Mohawk (Mkx)- pueden ser regulados al alza en respuesta a la carga sin que se produzcan cambios correspondientes en la expresión de Scx. Esto sugiere que la adaptación del tendón puede producirse independientemente de Scx y que su función principal puede estar relacionada con la formación temprana de las fibrillas más que con su posterior crecimiento. En cambio, la Mkx parece contribuir al agrandamiento y maduración de las fibrillas en respuesta a la estimulación mecánica, lo que respalda su papel en la adaptación estructural del tendón.
Los tendones adultos en fase de cicatrización suelen presentar características similares a las del tejido en desarrollo, como fibrillas de colágeno de pequeño diámetro y una elevada expresión de Scx. Sin embargo, a diferencia del desarrollo embrionario, la matriz de cicatrización no suele madurar hasta convertirse en tejido organizado y resistente. Una explicación es que las señales mecánicas no se transmitan adecuadamente a través de la matriz cicatrizada, un fenómeno coherente con el blindaje contra el estrés (que se analiza más adelante). Una señalización mecánica deficiente podría reducir la activación de vías mecanosensibles como Mkx, limitando la maduración de las fibrillas de colágeno y contribuyendo a la formación de tejido cicatricial mecánicamente inferior.
Compresión
Las fuerzas compresivas regulan la diferenciación de las células tendinosas y la composición de la matriz. Las regiones sometidas a compresión, como la entesis y las poleas del tendón, suelen desarrollar rasgos fibrocartilaginosos caracterizados por la expresión de marcadores de cartílago, como Col2a1 y aggrecan. Desde el punto de vista del desarrollo, los progenitores tendinosos coexpresan inicialmente Scx y Sox9 (un factor de transcripción condrogénico) antes de segregarse en células tendinosas adaptadas a la tensión y células de fibrocartílago adaptadas a la compresión. Evidencias experimentales muestran que la compresión sostenida puede inducir la formación de tejido similar al cartílago dentro del tendón, mientras que la carga de tensión promueve la expresión génica específica del tendón y suprime las vías condrogénicas. En ausencia de Mkx, la distensión puede favorecer paradójicamente la expresión de genes condrogénicos, lo que conduce a la formación ectópica de fibrocartílago. Estos hallazgos indican que las células del tendón poseen un potencial multipotente y que la carga mecánica gobierna la diferenciación a través de programas transcripcionales sensibles a la tensión y la compresión.
Esquilado
La lubricina y el ácido hialurónico son importantes mediadores del deslizamiento de los fascículos tendinosos y de la resistencia al cizallamiento. Sin embargo, su regulación biológica y su respuesta a la carga mecánica siguen estando insuficientemente caracterizadas, lo que limita la comprensión de su papel en la patología y la adaptación del tendón.
Disposición espacial
La organización del colágeno es esencial para la función del tendón y está fuertemente regulada por la tensión mecánica. Durante el desarrollo, las fuerzas de tracción alinean las células y las fibrillas de colágeno a través de estructuras especializadas (fibripositores), produciendo la arquitectura paralela característica de los tendones sanos. Incluso en las matrices de colágeno acelular, la distensión puede aumentar la alineación y la densidad de las fibrillas, y estos cambios pueden persistir tras la descarga. Sin embargo, la permanencia de la remodelación depende de la reticulación de la matriz, que puede reducir la adaptabilidad en tejidos envejecidos o metabólicamente alterados, como la diabetes. La carga de tracción también aumenta la resistencia a la degradación del colágeno y activa las vías bioquímicas (incluida la Mkx) que favorecen la maduración de las fibrillas. Por lo tanto, la adaptación del tendón refleja la interacción de la alineación mecánica pasiva y la señalización celular activa en respuesta a la carga mecánica. carga mecánicaun proceso que rige la remodelación estructural y la optimización funcional.
Las fuerzas ausentes y aberrantes intervienen en la degeneración de tendones y ligamentos
Los tendones en cicatrización a menudo se asemejan a tejidos inmaduros o embrionarios, mostrando una elevada expresión de Scx, un aumento de colágenos fibrilogénicos (III, V, XI), fibrillas de colágeno de pequeño diámetro, alta celularidad, vascularización y la presencia de progenitores Scx+/Sox9+. Estas características sugieren que el tendón lesionado reactiva un programa de desarrollo pero no progresa hacia la maduración mecánica completa, probablemente debido a una señalización mecánica alterada. La carga mecánica es esencial para la correcta regulación génica del tendón: la parálisis o la descarga reducen los factores de transcripción mecanosensibles clave, como Egr1, e interrumpen la señalización de Scx mediada por TGF-β, perjudicando la capacidad regenerativa. La carga de tracción favorece la expresión de genes específicos del tendón y suprime los genes del cartílago, mientras que la compresión o la descarga desplazan el equilibrio hacia fenotipos condrogénicos o degenerativos. Aunque el Colágeno III se asocia comúnmente con el tejido cicatricial, la evidencia de los modelos regenerativos muestra que su regulación temprana es parte de la reparación normal. La elevación persistente, especialmente en condiciones de descarga, refleja el fracaso de la maduración más que la causa de la degeneración. Incluso una mínima distensión mecánica es suficiente para regular la expresión génica de la matriz y mejorar la recuperación mecánica, poniendo de relieve la extrema sensibilidad de las células tendinosas a su entorno de carga. En conjunto, estos hallazgos sugieren que tanto las fuerzas mecánicas ausentes como las aberrantes interrumpen la progresión normal desde una matriz de reparación temprana hacia un tendón maduro y mecánicamente competente.
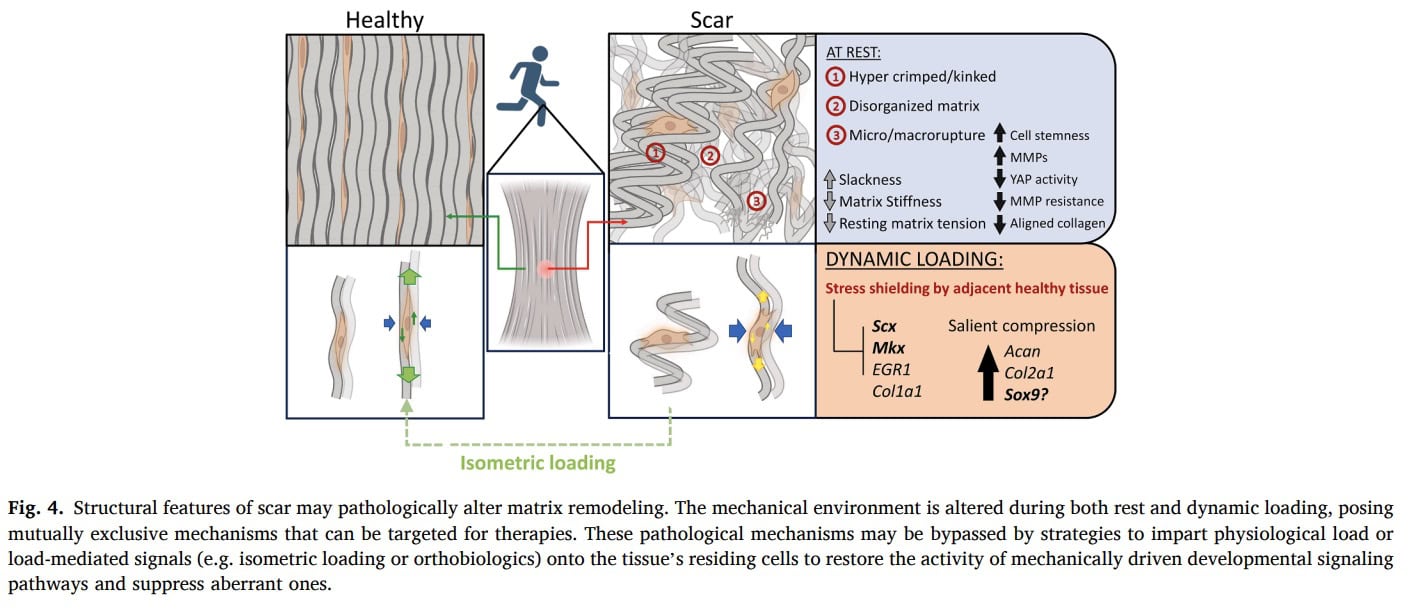
Protección contra el estrés
A medida que la tendinopatía progresa, las regiones degenerativas del tendón pueden volverse sintomáticas y estar sujetas a la protección contra el estrés. Cuando se aplica una carga mecánica, las porciones más rígidas y sanas del tendón soportan preferentemente la carga, mientras que las regiones degenerativas más flexibles se descargan. Este fenómeno biomecánico reduce aún más la estimulación mecánica del tejido enfermo y puede contribuir al desuso y al deterioro de la remodelación. Debido a que la porción degenerativa recibe poca carga efectiva, su capacidad de adaptación del tendón mediante carga mecánica está disminuida.
Los tendones muestran un comportamiento viscoelástico que puede aprovecharse terapéuticamente. Dos propiedades clave son la relajación del estrés -la disminución gradual de la tensión interna durante un estiramiento sostenido- y la fluencia, la deformación dependiente del tiempo de un tejido sometido a un estrés constante. Estas propiedades sugieren que las estrategias de carga controlada y sostenida pueden promover la estimulación mecánica de las regiones degenerativas a pesar del blindaje contra el estrés.
Las contracciones isométricas pueden representar una valiosa modalidad de carga. Los modelos experimentales han demostrado que la carga isométrica puede aumentar la expresión génica tenogénica. Las contracciones isométricas prolongadas pueden inducir la relajación del estrés en las regiones tendinosas más sanas, al tiempo que permiten la fluencia y la distensión mecánica en las zonas degenerativas. Esto podría facilitar la transmisión de la carga al tejido cicatrizado y favorecer potencialmente la adaptación biológica y estructural.
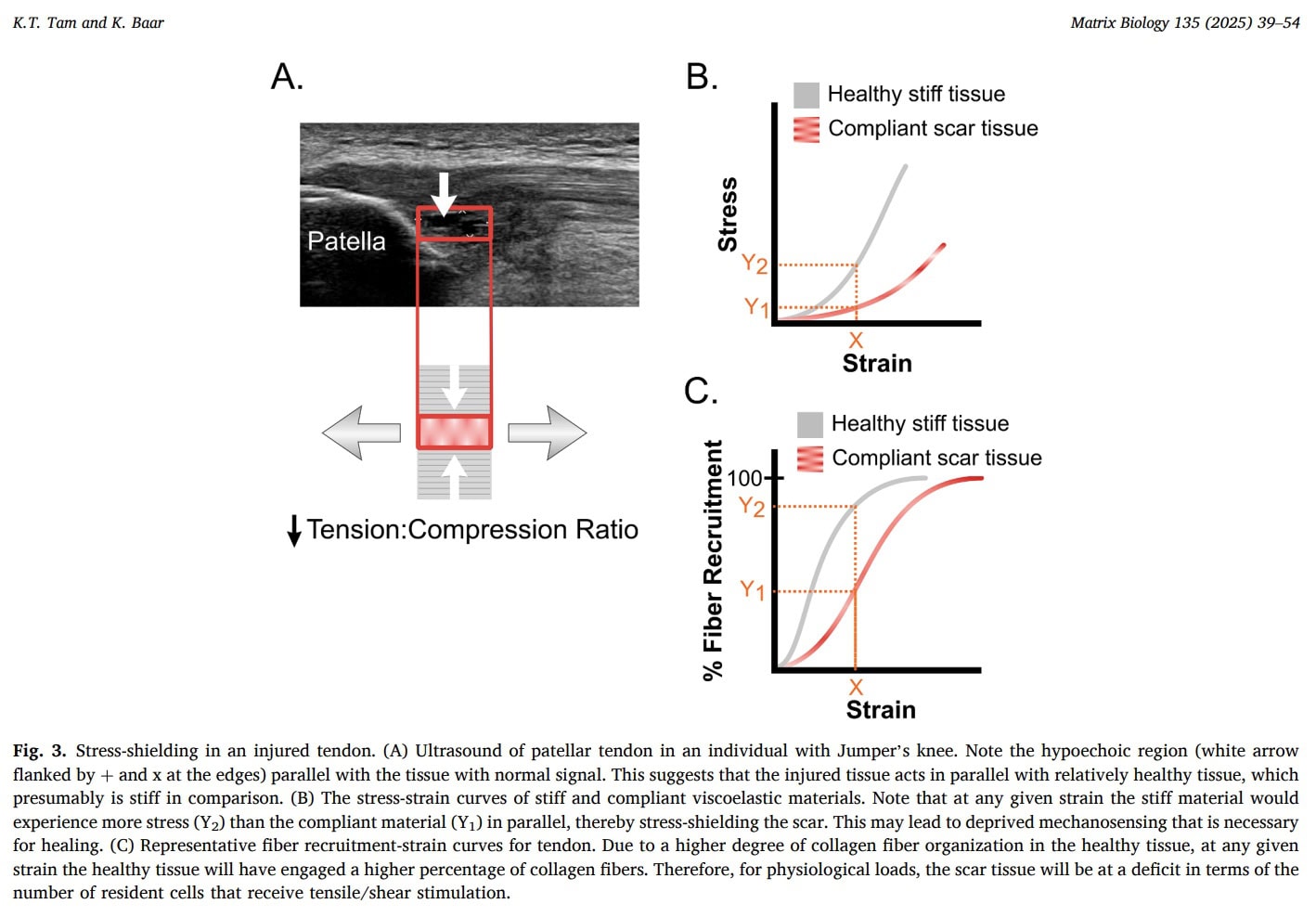
Preguntas y reflexiones
Tam et al. (2025) proponen que, en la tendinopatía, el tejido cicatricial flexible puede situarse en paralelo con el tendón sano más rígido y quedar mecánicamente "protegido contra la tensión", lo que significa que, a niveles fisiológicos normales de distensión, menos fibras de colágeno y células residentes dentro de la cicatriz experimentan realmente tensión de tracción. Dado que los reguladores tenogénicos clave son sensibles a la carga, una transmisión insuficiente del estrés puede impedir la maduración de la cicatriz y favorecer en cambio la persistencia de un fenotipo inmaduro o similar al fibrocartílago. Para la práctica clínica, este modelo respalda la justificación de la carga mecánica cuidadosamente dosificada en lugar de la descarga prolongada: se ha demostrado que la privación completa de estrés perjudica la expresión génica tenogénica y la recuperación mecánica. Los autores sugieren además que una carga sostenida que permita la fluencia viscoelástica (por ejemplo, contracciones isométricas) puede ayudar a transmitir tensión a la cicatriz y activar las vías tenogénicas, mientras que una carga inadecuada o ausente puede perpetuar la degeneración. Sin embargo, es importante destacar que, si bien este marco mecanobiológico proporciona una explicación plausible de por qué la carga controlada podría ser beneficiosa y por qué el miedo a todas las cargas puede estar fuera de lugar, la evidencia clínica directa de que las estrategias de carga específicas "superan" el blindaje contra el estrés en los seres humanos aún no se ha establecido en este documento.
La carga isométrica es una modalidad prometedora para la rehabilitación del tendón, pero los parámetros óptimos de entrenamiento siguen siendo inciertos. En este estudio de casose aplicó un programa combinado de carga isométrica y un protocolo de suplementación dietética a un atleta con tendinopatía rotuliana crónica. La estrategia dietética consistió en 15 g de gelatina con 225 mg de vitamina C consumidos aproximadamente una hora antes de las sesiones de entrenamiento, con el objetivo de favorecer la síntesis de colágeno.
El programa de ejercicios isométricos se centró en la carga del tendón de rango medio utilizando ejercicios de cadena abierta (extensión de piernas y prensa de piernas) y de cadena cerrada (sentadilla española). Las presiones isométricas se prescribieron inicialmente para 10 segundos y se aumentaron progresivamente en incrementos de 5 segundos hasta un máximo de 30 segundos. El volumen de entrenamiento oscilaba entre una y tres series de dos a cuatro repeticiones, realizadas a intensidades superiores al 80% del máximo de una repetición (1 RM), que se recalculaba mensualmente. Las sesiones duraron aproximadamente 10 minutos, con duraciones de mantenimiento elegidas basándose en evidencias que mostraban que la tensión del Tendón Rotuliano disminuye aproximadamente un 60% en 30 segundos de contracción sostenida y sólo marginalmente a partir de entonces.
Durante la intervención de 18 meses, los aumentos progresivos de la carga y la duración de la sujeción se asociaron con mejoras de la fuerza en todas las tareas resistidas (extensión de piernas, prensa de piernas y sujeciones de sentadilla española). Las imágenes por resonancia magnética (IRM) al inicio del estudio, a los 12 meses y a los 18 meses demostraron una reducción de la reactividad del tendón, un aumento del diámetro del tendón en la sustancia media y una disminución del grosor en los hallazgos de la inserción proximal, lo que concuerda con la remodelación estructural. El atleta informó de una reducción progresiva del dolor y no tenía dolor en el seguimiento de 18 meses.
Estas observaciones sugieren que el entrenamiento isométrico, especialmente cuando se combina con estrategias nutricionales que apoyan la síntesis de colágeno, puede promover la adaptación del tendón y la mejora de los síntomas. Sin embargo, la evidencia sigue limitándose a estudios experimentales e informes de casos aislados. Se necesitan ensayos controlados más amplios para determinar la eficacia y los parámetros óptimos de los protocolos isométricos. Además, las propiedades del tendón varían en función de la localización anatómica, el área de la sección transversal y el entorno mecánico, lo que puede influir en el comportamiento viscoelástico y las estrategias de carga adecuadas. Como se ha destacado a lo largo de esta revisión, el éxito de la rehabilitación depende probablemente de que se logre un equilibrio adecuado entre la subcarga y la carga excesiva, lo que subraya la necesidad de disponer de herramientas clínicas fiables para controlar la carga mecánica para la adaptación de los tendones. la carga mecánica para la adaptación del tendón.
Háblame de lo que es un "nerd
Aunque las revisiones narrativas están sujetas a sesgos inherentes, como el sesgo de selección, esta revisión proporciona un contexto biológico esencial que puede ayudar a los fisioterapeutas a comprender mejor la estructura del tendón y la mecanobiología en el tratamiento de la tendinopatía. El conocimiento de la regulación genética, las vías transcripcionales, la dinámica de los aminoácidos y la remodelación de las proteínas contribuye a una comprensión más profunda de la cicatrización y adaptación del tendón, que puede servir de base a las estrategias de rehabilitación. Sin embargo, la mayoría de las evidencias mecanicistas proceden de modelos animales, y la extrapolación directa a la patología del tendón humano sigue siendo limitada.
Aunque se necesitan ensayos clínicos más avanzados para reforzar la base de pruebas, en el siguiente artículo de esta serie se examinarán los datos de un estudio de 2022 en el que se investiga un protocolo de ejercicio de alta carga dirigido a aumentar el área transversal del tendón y mejorar el dolor y la función en pacientes con tendinopatía de Aquiles.
Mensajes para llevar a casa
- Los tendones son tejidos vivos y adaptables. Responden a la carga mecánica a través de la señalización celular y la remodelación de la matriz. Los estímulos mecánicos impulsan la adaptación estructural: los tendones no son estructuras inertes.
- La carga biomecánica es esencial para la adaptación. Un estrés mecánico adecuado promueve la salud y la remodelación del tendón, favoreciendo la recuperación funcional y la mejora estructural mediante carga mecánica en la adaptación del tendón.
- El blindaje contra el estrés limita la adaptación. Las regiones tendinosas degenerativas pueden descargarse cuando el tejido sano soporta la mayor parte de la carga mecánica. Esto reduce la estimulación mecánica efectiva y puede dificultar la recuperación.
- La rehabilitación debe superar el blindaje contra el estrés. Las estrategias de carga deben tener como objetivo transmitir fuerzas mecánicas a los tejidos degenerativos, evitando al mismo tiempo una distensión excesiva. Las propiedades viscoelásticas (relajación del estrés y fluencia) proporcionan una base biomecánica para la carga terapéutica controlada.
- Una carga equilibrada es la clave. Los tendones requieren un estímulo mecánico suficiente para la adaptación, pero son vulnerables a la infracarga (que perpetúa el desuso) y a la sobrecarga (que puede agravar los síntomas). La carga individualizada y progresiva es esencial.
- Implicaciones clínicas para la fisioterapia. La rehabilitación debe centrarse en estrategias de carga mensurables y progresivas que devuelvan la estimulación mecánica al tejido enfermo y aprovechen la adaptabilidad del tendón.
- Próximos pasos. El próximo artículo traducirá estos principios biomecánicos en estrategias clínicas, revisando protocolos de ejercicio de alta carga y enfoques prácticos para optimizar la adaptación del tendón, la reducción del dolor y la recuperación funcional en la tendinopatía.
Este recurso de Physiotutors proporciona perspectivas adicionales sobre la biología del tendón y la mecanobiología, ofreciendo conocimientos clínicamente relevantes sobre la función y adaptación del tendón.
Referencia
EL PAPEL DE LA VMO Y LOS QUADS EN LA PFP
Mira esto VIDEO CONFERENCIA GRATUITA DE 2 PARTES por un experto en dolor de rodilla Claire Robertson que disecciona la literatura sobre el tema y cómo se impacto en la práctica clínica.