Wpływ obciążeń mechanicznych na adaptację ścięgien - biologiczne podstawy precyzyjnych interwencji w terapii wysiłkowej
Wprowadzenie
Pomimo postępów w naszym rozumieniu patogenezy tendinopatii, wyniki po tradycyjnych interwencjach zachowawczych i medycznych pozostają niespójne, a wielu pacjentów doświadcza uporczywego bólu i ograniczeń funkcjonalnych. Powszechnie cytowany model kontinuum zaproponowany przez Jill Cook sugeruje, że zwyrodnieniowa część ścięgna jest strukturalnie nieodwracalna. Jednak pojawiające się dowody strukturalne i mechanobiologiczne podważają to założenie, wskazując, że tkanka ścięgna może zachować większą zdolność do adaptacji i przebudowy niż wcześniej sądzono.
Niniejszy przegląd bada wpływ obciążenia mechanicznego na adaptację ścięgien i mechanizmy biologiczne leżące u podstaw zwyrodnienia, ze szczególnym uwzględnieniem sygnalizacji komórkowej, przebudowy macierzy i szlaków mechanotransdukcji. Poprzez integrację najnowszych wyników badań eksperymentalnych, ma ona na celu zapewnienie biologicznie ugruntowanych ram do informowania o zaleceniach dotyczących ćwiczeń w leczeniu tendinopatii. Ta teoretyczna synteza służy jako podstawa dla nadchodzącego przeglądu badającego strategie ćwiczeń z dużym obciążeniem i wprowadzającego nowy protokół obciążenia tendinopatii do zastosowania klinicznego.
Metody
Ten opisowy przegląd syntetyzuje wyniki wielu badań eksperymentalnych, przeprowadzonych głównie na modelach zwierzęcych.
Wyniki
Biologiczne podstawy struktury Ścięgna
Kolagen typu I (COL1/Col1a1) jest głównym białkiem strukturalnym tkanki ścięgien i więzadeł, nadającym wytrzymałość na rozciąganie. Po urazie synteza kolagenu wzrasta, jednak odkładanie macierzy podczas fazy proliferacyjnej jest często zdezorganizowane. Podczas gdy zdrowe ścięgna wykazują włókna kolagenu ułożone równolegle do sił mechanicznych, patologiczne ścięgna zawierają mniejsze, mniej usieciowane i zdezorganizowane włókna. Chociaż kolagen typu I zapewnia lepszą odporność mechaniczną w porównaniu z kolagenem typu III, gojenie ścięgien często zawiera większą ilość kolagenu typu III. Metaloproteinazy macierzy (MMP), enzymy odpowiedzialne za degradację kolagenu, są jednocześnie aktywne podczas przebudowy tkanki.
WYNIK Ścięgna dorosłych osób po urazach zwykle stają się wysoce komórkowe i rozwijają zdezorganizowaną macierz kolagenową charakteryzującą się włóknami o małej średnicy, w wyniku czego powstaje fenotyp tkanki zwyrodnieniowej.
Regeneracja tkanek i rekapitulacja rozwojowa
W odpowiedzi na urazy, geny normalnie aktywne podczas rozwoju embrionalnego ulegają ponownej ekspresji. Populacje komórek macierzystych i proliferacyjnych rozszerzają się i różnicują w wyspecjalizowane tkanki; jednak dorosłe ścięgna zazwyczaj nie regenerują się w pełni, często pozostawiając resztkową macierz degeneracyjną. Z kolei modele noworodkowe wykazują większą zdolność do funkcjonalnej naprawy, z organizacją tkanki przypominającą procesy rozwojowe. Odkrycia te sugerują, że zdolność regeneracyjna może zależeć od zdolności do odtwarzania programów rozwojowych, która to cecha wydaje się być silniejsza u młodszych organizmów i niektórych modeli eksperymentalnych niż w gojeniu się ścięgien u dorosłych ludzi.
Właściwości materiału odzwierciedlają wymagania mechaniczne
Ścięgna można sklasyfikować zgodnie z ich funkcją mechaniczną jako struktury magazynujące energię lub pozycjonujące. Ścięgna magazynujące energię, takie jak Ścięgno Achillesa, pochłaniają i zwracają energię mechaniczną w celu zwiększenia wydajności lokomotorycznej. Ścięgna pozycyjne, których przykładem jest ścięgno piszczelowe przednie, przede wszystkim pozycjonują stawy i ułatwiają ruchy, takie jak prześwit stopy podczas chodu. Te funkcjonalne różnice znajdują odzwierciedlenie we właściwościach strukturalnych: ścięgna magazynujące energię mają zazwyczaj większy przekrój poprzeczny, kompensując niższą sztywność materiału, aby umożliwić elastyczne magazynowanie energii. Ścięgna w obrębie tego samego łańcucha kinetycznego mogą również wykazywać różne mechanizmy. Na przykład, ścięgno mięśnia czworogłowego i ścięgno rzepki działają szeregowo, ale wykazują różne właściwości sztywności, przy czym ścięgno mięśnia czworogłowego jest około dwa razy mniej sztywne. Różnica ta prawdopodobnie odzwierciedla ich mechanizmy - wprowadzenie do kości w przypadku ścięgna rzepki w porównaniu z przyczepem mięsień-kość w przypadku ścięgna czworogłowego - które narzucają różne wzorce obciążenia, a tym samym wpływają na obciążenie mechaniczne podczas adaptacji ścięgna i wymagania materiałowe. obciążenie mechaniczne na adaptację ścięgna i wymagania materiałowe.
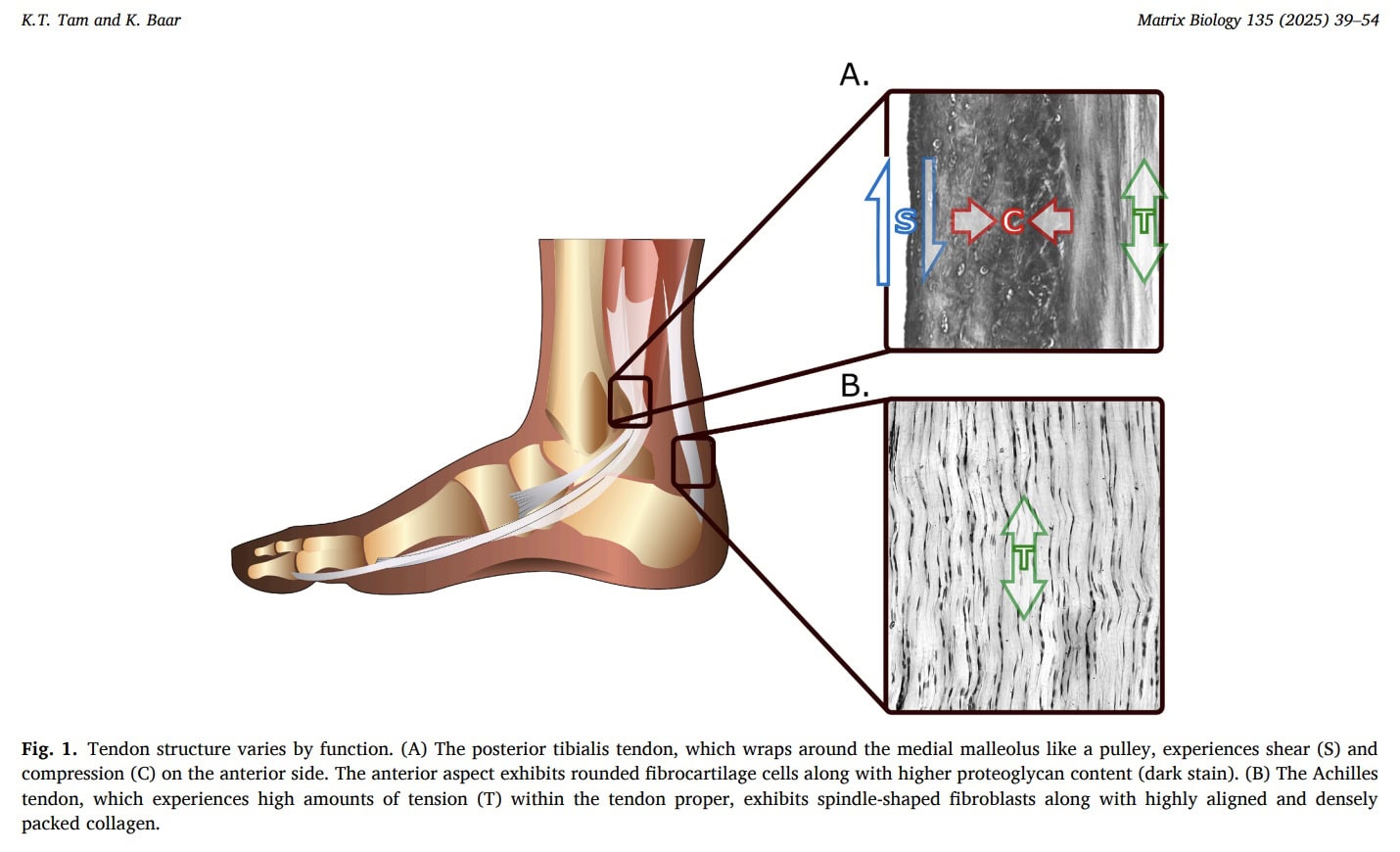
Kompresja
Siły ściskające często działają na ścięgna, szczególnie tam, gdzie owijają się one wokół struktur kostnych lub siatkowatych. Badania eksperymentalne na modelach zwierzęcych pokazują, że usunięcie obciążenia ściskającego zmniejsza sztywność ścięgien i zmienia adaptację strukturalną, wskazując, że ścięgna narażone na ściskanie przebudowują się, aby dostosować się do tego mechanicznego środowiska. U ludzi obszary ścięgien poddane kompresji często wykazują cechy włóknisto-chrzęstne bogate w kolagen typu II, wyspecjalizowany do przeciwstawiania się siłom ściskającym.
Shear
Siły ścinające powstają w wyniku względnego poślizgu między ścięgnami, więzadłami, mięśniami i sąsiednimi tkankami. W Ścięgnie Achillesa zróżnicowany poślizg pomiędzy ścięgnami ułatwia przenoszenie siły, ale może zmniejszać się wraz z wiekiem, potencjalnie przyczyniając się do zmniejszenia Zakresu ruchu i upośledzonego rozkładu siły. Spadek zdolności ślizgowych może częściowo wyjaśniać częstsze występowanie zerwania ścięgna achillesa u osób starszych. Podobnie jak w przypadku adaptacji kompresyjnej, zmniejszone obciążenie mechaniczne może przyczyniać się do zmian zwyrodnieniowych, zwiększonego ryzyka urazów i dezadaptacji.
Określone siły napędzają określone programy molekularne
Na losy komórek i skład tkanki silny wpływ ma środowisko mechaniczne poprzez szlaki mechanotransdukcji, podkreślając znaczenie obciążenia mechanicznego na adaptację ścięgna. obciążenia mechanicznego na adaptację ścięgien.. Mechanizmy mechaniczne inicjują biologiczne i metaboliczne adaptacje, które regulują strukturę i funkcję tkanek, choć specyficzne szlaki regulujące gojenie się ścięgien pozostają nie do końca poznane. W kolejnych rozdziałach przeanalizowano biomechaniczny wpływ różnych rodzajów obciążeń na adaptację i naprawę ścięgien.
Napięcie
Manipulowanie środowiskiem mechanicznym, w tym obciążeniem mechanicznymma kluczowe znaczenie dla przebudowy ścięgien i adaptacji funkcjonalnej. Obciążenie rozciągające napędza przebudowę tkanek, ale równowaga między korzystnymi i potencjalnie szkodliwymi obciążeniami pozostaje kluczowa. Lepsze zrozumienie biomechaniki strategii obciążania jest zatem niezbędne do optymalizacji rehabilitacji i adaptacji ścięgien.
Scleraxis (Scx) jest kluczowym czynnikiem transkrypcyjnym zaangażowanym w rozwój ścięgien i regulację kolagenu. Podczas embriogenezy Scx promuje syntezę kolagenu typu I (COL1) poprzez wiązanie się z regionami regulatorowymi genu Col1a1. Na jego ekspresję wpływa aktywność mięśni i obciążenie mechaniczne. Jednak w dorosłych ścięgnach Scx wydaje się mniej istotny dla wzrostu adaptacyjnego. Kilka genów tenogennych - w tym Col1a1, tenomodulina (Tnmd), fibromodulina (Fmod) i Mohawk (Mkx) - może być regulowanych w górę w odpowiedzi na obciążenie bez odpowiednich zmian w ekspresji Scx. Sugeruje to, że adaptacja ścięgien może zachodzić niezależnie od Scx, a jego główna rola może odnosić się do wczesnego tworzenia fibryli, a nie ich późniejszego wzrostu. Z kolei Mkx wydaje się przyczyniać do powiększania i dojrzewania fibryli w odpowiedzi na stymulację mechaniczną, wspierając swoją rolę w adaptacji strukturalnej ścięgien.
Gojenie dorosłych ścięgien często wykazuje cechy przypominające tkankę rozwojową, w tym włókna kolagenu o małej średnicy i podwyższoną ekspresję Scx. Jednak w przeciwieństwie do rozwoju embrionalnego, macierz gojenia często nie dojrzewa do zorganizowanej, nośnej tkanki. Jednym z wyjaśnień jest to, że sygnały mechaniczne mogą nie być odpowiednio przekazywane przez bliznowatą macierz, co jest zjawiskiem zgodnym z ekranowaniem naprężeń (omówionym poniżej). Upośledzona sygnalizacja mechaniczna może zmniejszać aktywację szlaków mechanowrażliwych, takich jak Mkx, ograniczając dojrzewanie włókien kolagenu i przyczyniając się do powstawania mechanicznie gorszej tkanki bliznowatej.
Kompresja
Siły ściskające regulują różnicowanie komórek ścięgien i skład macierzy. Obszary poddane kompresji - takie jak enteza i krążki ścięgien - często rozwijają cechy włóknisto-chrzęstne charakteryzujące się ekspresją markerów chrząstki, w tym Col2a1 i agrekanu. Rozwojowo, progenitory ścięgien początkowo wykazują koekspresję Scx i Sox9 (chondrogenny czynnik transkrypcyjny) przed segregacją na komórki ścięgien przystosowane do rozciągania i komórki chrząstki włóknistej przystosowane do ściskania. Dowody eksperymentalne wskazują, że długotrwałe ściskanie może indukować tworzenie tkanki podobnej do chrząstki w obrębie ścięgna, podczas gdy obciążenie rozciągające promuje ekspresję genów specyficznych dla ścięgna i tłumi szlaki chondrogenne. W przypadku braku Mkx, naderwanie może paradoksalnie sprzyjać ekspresji genów chondrogennych, prowadząc do ektopowego tworzenia chrząstki włóknistej. Wyniki te wskazują, że komórki ścięgien posiadają potencjał multipotencjalny i że obciążenie mechaniczne reguluje różnicowanie poprzez programy transkrypcyjne wrażliwe na napięcie i ściskanie.
Ścinanie
Lubrycyna i kwas hialuronowy są ważnymi mediatorami poślizgu ścięgien i odporności na ścinanie. Jednak ich regulacja biologiczna i odpowiedź na obciążenia mechaniczne pozostają niewystarczająco scharakteryzowane, co ogranicza zrozumienie ich roli w patologii i adaptacji ścięgien.
Układ przestrzenny
Organizacja kolagenu jest niezbędna dla funkcjonowania ścięgien i jest silnie regulowana przez napięcie mechaniczne. Podczas rozwoju, siły rozciągające wyrównują komórki i włókna kolagenu poprzez wyspecjalizowane struktury (fibripository), tworząc równoległą architekturę charakterystyczną dla zdrowych ścięgien. Nawet w bezkomórkowych matrycach kolagenowych, naderwanie może zwiększyć ułożenie i gęstość włókien, a zmiany te mogą uporczywie utrzymywać się po odciążeniu. Trwałość przebudowy zależy jednak od sieciowania macierzy, co może zmniejszać zdolność adaptacji w starzejących się lub metabolicznie zmienionych tkankach, takich jak cukrzyca. Obciążenie rozciągające zwiększa również odporność na degradację kolagenu i aktywację szlaków biochemicznych (w tym Mkx), które wspierają dojrzewanie fibryli. Adaptacja ścięgna odzwierciedla zatem interakcję pasywnego wyrównania mechanicznego i aktywnej sygnalizacji komórkowej w odpowiedzi na obciążenie mechaniczne, proces, który reguluje przebudowę strukturalną i optymalizację funkcjonalną. obciążenie mechaniczne MECHANIZMproces, który reguluje przebudowę strukturalną i optymalizację funkcjonalną.
Nieobecne i nieprawidłowe siły odgrywają rolę w zwyrodnieniu ścięgien i więzadeł.
Gojenie się ścięgien często przypomina niedojrzałą lub embrionalną tkankę, wykazując podwyższoną ekspresję Scx, zwiększoną ilość fibrylogennych kolagenów (III, V, XI), fibryle kolagenowe o małej średnicy, wysoką komórkowość, unaczynienie i obecność progenitorów Scx+/Sox9+. Cechy te sugerują, że uszkodzone ścięgno reaktywuje program rozwojowy, ale nie osiąga progresji w kierunku pełnego dojrzewania mechanicznego, prawdopodobnie z powodu zmienionej sygnalizacji mechanicznej. Obciążenie mechaniczne jest niezbędne do prawidłowej regulacji genów ścięgna: paraliż lub odciążenie zmniejsza kluczowe mechanowrażliwe czynniki transkrypcyjne, takie jak Egr1 i zakłóca sygnalizację Scx za pośrednictwem TGF-β, upośledzając zdolność regeneracji. Ścięgno poddane obciążeniu promuje ekspresję genów specyficznych dla ścięgna, jednocześnie tłumiąc geny chrząstki, podczas gdy ściskanie lub odciążanie przesuwa równowagę w kierunku fenotypów chondrogennych lub zwyrodnieniowych. Chociaż kolagen III jest powszechnie kojarzony z tkanką bliznowatą, dowody z modeli regeneracyjnych wskazują, że jego wczesna regulacja jest częścią normalnej naprawy. Uporczywy wzrost, szczególnie w warunkach odciążenia, odzwierciedla raczej nieudane dojrzewanie niż przyczynę zwyrodnienia. Nawet minimalne obciążenie mechaniczne jest wystarczające do regulacji ekspresji genów macierzy i poprawy mechanicznego powrotu do zdrowia, podkreślając sensytyzację komórek ścięgna do ich środowiska obciążenia. Łącznie wyniki te sugerują, że zarówno nieobecne, jak i nieprawidłowe siły mechaniczne zakłócają normalną progresję od wczesnej macierzy naprawczej w kierunku dojrzałego, mechanicznie kompetentnego ścięgna.
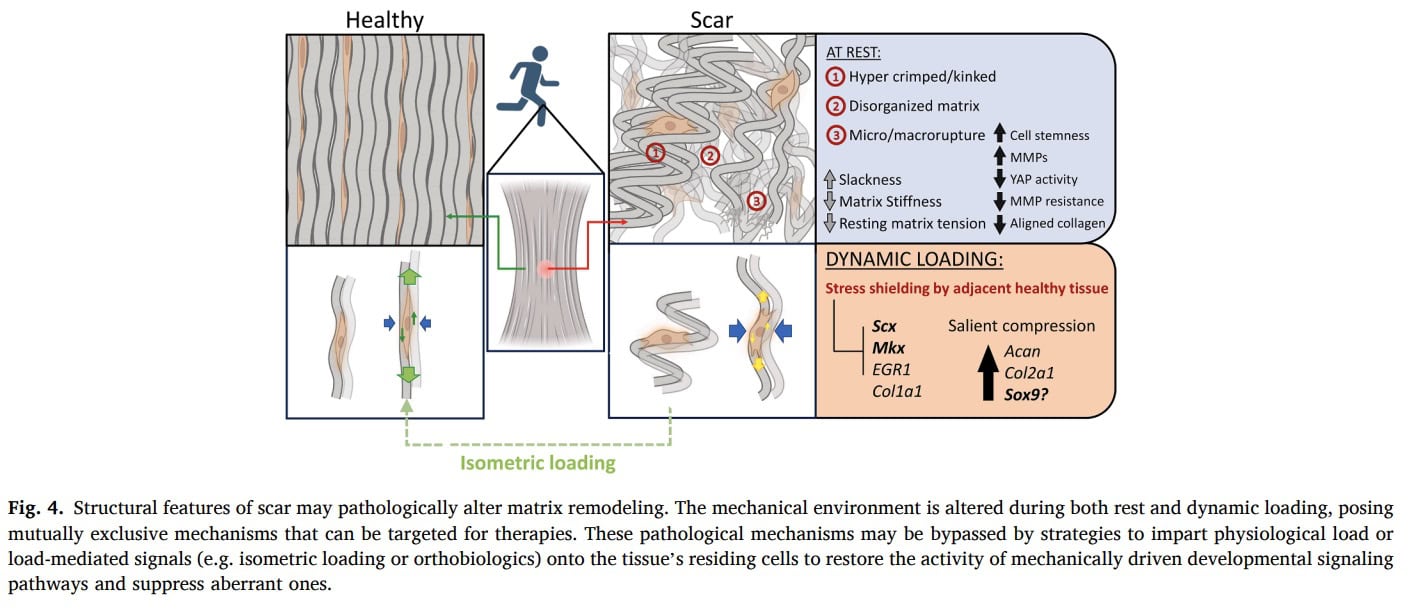
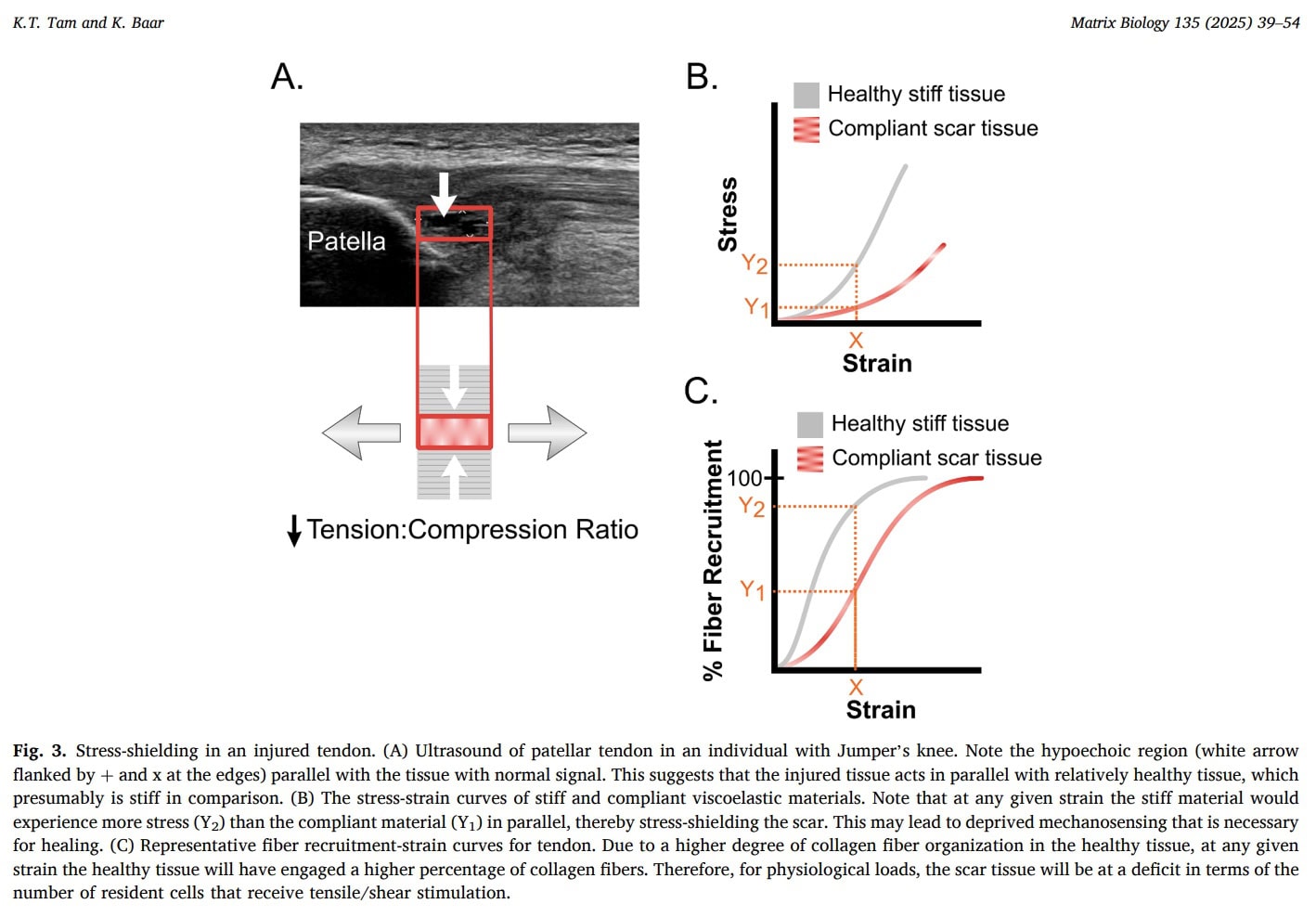
Ochrona przed stresem
W miarę progresji tendinopatii, zwyrodniałe obszary ścięgien mogą stać się objawowe i podlegać ochronie przed naprężeniami. Gdy stosowane jest obciążenie mechaniczne, sztywniejsze i zdrowsze części ścięgna preferencyjnie przenoszą obciążenie, podczas gdy bardziej podatne obszary zwyrodnieniowe są odciążane. To zjawisko biomechaniczne dodatkowo zmniejsza mechaniczną stymulację chorej tkanki i może przyczyniać się do jej nieużywania i upośledzonej przebudowy. Ponieważ część zwyrodnieniowa otrzymuje niewielkie efektywne obciążenie, jej zdolność do adaptacji ścięgna poprzez obciążenie mechaniczne jest zmniejszona. obciążenie mechaniczne jest zmniejszona.
Ścięgna wykazują właściwości lepkosprężyste, które można wykorzystać terapeutycznie. Dwie kluczowe właściwości to relaksacja naprężeń - stopniowy spadek napięcia wewnętrznego podczas długotrwałego rozciągania - oraz pełzanie, zależne od czasu odkształcenie tkanki pod stałym naprężeniem. Właściwości te sugerują, że kontrolowane, długotrwałe strategie obciążania mogą promować mechaniczną stymulację obszarów zwyrodnieniowych pomimo ekranowania naprężeń.
Skurcze izometryczne mogą stanowić cenną metodę obciążania. Modele eksperymentalne wykazały, że obciążenie izometryczne może zwiększać ekspresję genów tenogennych. Przedłużone skurcze izometryczne mogą indukować relaksację naprężeń w zdrowszych obszarach ścięgien, jednocześnie umożliwiając pełzanie i odkształcenia mechaniczne w obszarach zwyrodnieniowych. Może to ułatwić przenoszenie obciążeń na bliznowatą tkankę i potencjalnie wspierać adaptację biologiczną i strukturalną.
Pytania i przemyślenia
Tam i wsp. (2025) proponują, że w tendinopatii podatna tkanka bliznowata może znajdować się równolegle do sztywniejszego zdrowego ścięgna i stać się mechanicznie "osłonięta przed naprężeniami", co oznacza, że przy normalnych fizjologicznych poziomach naderwania mniej włókien kolagenowych i komórek rezydujących w bliźnie faktycznie doświadcza naprężeń rozciągających. Ponieważ kluczowe regulatory tenogeniczne są czułe na obciążenie, niewystarczające przenoszenie stresu może zapobiegać dojrzewaniu blizny i zamiast tego sprzyjać uporczywemu niedojrzałemu lub włóknisto-chrzęstnemu fenotypowi. Z punktu widzenia praktyki klinicznej, model ten potwierdza zasadność ostrożnego dozowania obciążenia mechanicznego zamiast długotrwałego rozładunku: wykazano, że całkowite pozbawienie stresu osłabia ekspresję genów tenogennych i powrót do zdrowia. Autorzy sugerują ponadto, że długotrwałe obciążenie pozwalające na pełzanie lepkosprężyste (np. skurcze izometryczne) może pomóc w przenoszeniu napięcia do blizny i aktywacji szlaków tenogenicznych, podczas gdy niewłaściwe obciążenie lub jego brak może utrwalić zwyrodnienie. Ważne jest jednak, aby podkreślić, że chociaż te ramy mechanobiologiczne dostarczają wiarygodnego wyjaśnienia, dlaczego kontrolowane obciążenie może być korzystne i dlaczego strach przed wszelkim obciążeniem może być nieuzasadniony, bezpośrednie dowody kliniczne, że określone strategie obciążenia "pokonują" ekranowanie stresu u ludzi, nie zostały jeszcze ustalone w tym artykule.
Obciążenie izometryczne jest obiecującą metodą rehabilitacji ścięgien, ale optymalne parametry treningowe pozostają niepewne. W tym studium przypadkuu sportowca z przewlekłą tendinopatią rzepki zastosowano połączony program obciążenia izometrycznego i suplementacji diety. Strategia żywieniowa polegała na spożywaniu 15 g żelatyny z 225 mg witaminy C na około godzinę przed sesjami treningowymi w celu wsparcia syntezy kolagenu.
Program ćwiczeń izometrycznych ukierunkowany był na obciążenie ścięgna w średnim zakresie przy użyciu zarówno ćwiczeń w otwartym łańcuchu (wyprost nóg i wyciskanie nogami), jak i ćwiczeń w zamkniętym łańcuchu (przysiad hiszpański). Przytrzymania izometryczne były początkowo zalecane przez 10 sekund i stopniowo zwiększane o 5-sekundowe przyrosty do maksymalnie 30 sekund. Objętość treningu wahała się od jednego do trzech zestawów po dwa do czterech powtórzeń, wykonywanych z intensywnością przekraczającą 80% maksymalnego obciążenia dla jednego powtórzenia (1 RM), które było przeliczane co miesiąc. Sesje trwały około 10 minut, a czas trwania wstrzymania wybrano na podstawie dowodów wskazujących, że napięcie ścięgna rzepki zmniejsza się o około 60% w ciągu 30 sekund trwałego skurczu i tylko nieznacznie później.
W ciągu 18-miesięcznej interwencji stopniowe zwiększanie obciążenia i czasu trwania przytrzymania wiązało się z poprawą siły we wszystkich zadaniach wymagających oporu (wyprost nóg, wyciskanie nogami i hiszpańskie przytrzymanie w przysiadzie). Rezonans magnetyczny (MRI) na początku badania, po 12 miesiącach i po 18 miesiącach wykazał zmniejszenie reaktywności ścięgna, zwiększenie średnicy ścięgna w części przyśrodkowej i zmniejszenie grubości w części proksymalnej, co wskazuje na przebudowę strukturalną. Zawodnik zgłosił progresję bólu i był wolny od bólu podczas 18-miesięcznej obserwacji.
Obserwacje te sugerują, że trening izometryczny, szczególnie w połączeniu ze strategiami odżywiania wspierającymi syntezę kolagenu, może promować adaptację ścięgien i poprawę objawów. Dowody pozostają jednak ograniczone do badań eksperymentalnych i pojedynczych opisów przypadków. W celu określenia skuteczności i optymalnych parametrów protokołów izometrycznych wymagane są większe kontrolowane badania. Dodatkowo, właściwości ścięgien różnią się w zależności od lokalizacji anatomicznej, powierzchni przekroju poprzecznego i środowiska mechanicznego, co może wpływać na zachowanie lepkosprężyste i odpowiednie strategie obciążania. Jak podkreślono w niniejszym przeglądzie, skuteczna rehabilitacja prawdopodobnie zależy od osiągnięcia odpowiedniej równowagi między niedociążeniem a nadmiernym obciążeniem, podkreślając potrzebę niezawodnych narzędzi klinicznych do monitorowania obciążenia mechanicznego w celu adaptacji ścięgna. obciążenia mechanicznego w celu adaptacji ścięgien.
Porozmawiaj ze mną
Chociaż przeglądy narracyjne podlegają nieodłącznym uprzedzeniom, takim jak tendencyjność selekcji, niniejszy przegląd zapewnia istotny kontekst biologiczny, który może pomóc fizjoterapeutom lepiej zrozumieć strukturę ścięgien i mechanobiologię w leczeniu tendinopatii. Wiedza na temat regulacji genetycznej, szlaków transkrypcyjnych, dynamiki aminokwasów i przebudowy białek przyczynia się do głębszego zrozumienia gojenia i adaptacji ścięgien, co może wpływać na strategie rehabilitacji. Jednak większość dowodów mechanistycznych pochodzi z modeli zwierzęcych, a bezpośrednia ekstrapolacja na patologię ścięgien u ludzi pozostaje ograniczona.
Podczas gdy do wzmocnienia bazy dowodowej potrzebne są bardziej zaawansowane badania kliniczne, w kolejnym artykule z tej serii przeanalizujemy dane z badania z 2022 r. dotyczącego protokołu ćwiczeń z dużym obciążeniem, mającego na celu zwiększenie pola przekroju ścięgna oraz poprawę bólu i funkcji u pacjentów z TENDINOPATIĄ ŚCIĘGNA ACHILLESA.
Przesłania na przyszłość
- Ścięgna są żywymi, adaptacyjnymi tkankami. Reagują na obciążenia mechaniczne poprzez sygnalizację komórkową i przebudowę macierzy. Bodźce mechaniczne napędzają adaptację strukturalną - ścięgna nie są strukturami obojętnymi.
- Obciążenie biomechaniczne jest niezbędne do adaptacji. Odpowiednie obciążenie mechaniczne promuje zdrowie i przebudowę ścięgien, wspierając powrót do zdrowia i poprawę strukturalną poprzez mechanicznemu obciążeniu adaptacji ścięgien..
- Osłona przed stresem ogranicza adaptację. Zwyrodniałe obszary ścięgien mogą być odciążone, gdy zdrowsza tkanka przenosi większość obciążenia mechanicznego. Zmniejsza to skuteczną stymulację mechaniczną i może utrudniać powrót do zdrowia.
- Rehabilitacja musi przezwyciężyć ekranowanie naprężeń. Strategie obciążania powinny mieć na celu przenoszenie sił mechanicznych na zwyrodniałą tkankę przy jednoczesnym unikaniu nadmiernego naderwania. Właściwości lepkosprężyste (relaksacja naprężeń i pełzanie) stanowią biomechaniczną podstawę kontrolowanych obciążeń terapeutycznych.
- Równowaga obciążeń jest kluczowa. Ścięgna wymagają wystarczających bodźców mechanicznych do adaptacji, ale są podatne na niedociążenie (które utrwala nieużywanie) i przeciążenie (które może nasilać objawy). Zindywidualizowane, progresywne obciążenie jest niezbędne.
- Implikacje kliniczne dla fizjoterapii. Rehabilitacja powinna koncentrować się na wymiernych i progresywnych strategiach obciążenia, które przywracają mechaniczną stymulację chorej tkanki i wykorzystują zdolności adaptacyjne ścięgien.
- Kolejne kroki. Nadchodzący artykuł przełoży te zasady biomechaniki na strategie kliniczne, dokonując przeglądu protokołów ćwiczeń z dużym obciążeniem i praktycznych podejść do optymalizacji adaptacji ścięgien, redukcji bólu i powrotu do zdrowia w przypadku tendinopatii.
Ten zasób od Physiotutors zapewnia dodatkowe spojrzenie na biologię ścięgien i mechanobiologię, oferując klinicznie istotne spojrzenie na funkcję i adaptację ścięgien.
Odniesienie
ROLA VMO I QUADÓW W PFP
Obejrzyj ten BEZPŁATNY 2-CZĘŚCIOWY WYKŁAD WIDEO eksperta ds. bólu kolana Claire Robertson, który analizuje literaturę na ten temat i jej wpływ na praktykę kliniczną.