A mechanikai terhelés hatása az ín adaptációjára - a precíz mozgásterápiás beavatkozások biológiai háttere
Bemutatkozás
Annak ellenére, hogy az íngyulladás patogeneziseinek megértésében előrelépés történt, a hagyományos konzervatív és orvosi beavatkozásokat követő eredmények továbbra is ellentmondásosak, sok betegnél perzisztens fájdalom és funkcionális korlátozások tapasztalhatók. A Jill Cook által javasolt, széles körben idézett kontinuum modell azt sugallja, hogy az ín degeneratív része szerkezetileg irreverzibilis. Az új strukturális és mechanobiológiai bizonyítékok azonban megkérdőjelezik ezt a feltételezést, és arra utalnak, hogy az ínszövet a korábban gondoltnál nagyobb adaptációs és átalakulási képességet tarthat fenn.
Ez az áttekintés a következők hatását vizsgálja mechanikai terhelés az ín adaptációjára és a degeneráció hátterében álló biológiai mechanizmusokat, különös tekintettel a sejtes jelátvitelre, a mátrix átalakulására és a mechanotranszdukciós útvonalakra. A legújabb kísérleti eredmények integrálásával célja, hogy biológiailag megalapozott keretet biztosítson az íngyulladás kezelésében alkalmazott edzésre vonatkozó előírásokhoz. Ez az elméleti szintézis szolgál alapjául egy hamarosan megjelenő áttekintésnek, amely a nagy terhelésű edzésstratégiákat vizsgálja, és egy új, klinikai alkalmazásra szánt íngyulladásos terhelési protokollt vezet be.
Módszerek
Ez a narratív áttekintés több, túlnyomórészt állatmodellekben végzett kísérleti vizsgálat eredményeit összegzi.
Eredmények
Az ín szerkezet biológiai alapja
Az I. típusú kollagén (COL1/Col1a1) az ín- és szalagszövetek fő szerkezeti fehérjéje, amely a húzószilárdságot biztosítja. Sérülést követően a kollagénszintézis fokozódik; a proliferatív fázisban azonban a mátrix lerakódása gyakran rendezetlen. Míg az egészséges inak a mechanikai erőkkel párhuzamosan igazodó kollagénfibrillumokat mutatnak, a patológiai inak kisebb, kevésbé térhálósodott és rendezetlen fibrillumokat tartalmaznak. Bár az I. típusú kollagén jobb mechanikai terhelést biztosít a III. típusú kollagénhez képest, a gyógyuló ínök gyakran nagyobb arányban tartalmaznak III. típusú kollagént. A mátrix metalloproteinázok (MMP-k), a kollagén lebontásáért felelős enzimek, egyidejűleg aktívak a szöveti remodelling során.
A sérült felnőtt ínszövetek jellemzően erősen sejtszintűvé válnak, és kis átmérőjű fibrillákkal jellemezhető, dezorganizált kollagénmátrixot alakítanak ki, ami degeneratív szövetfenotípust eredményez.
Szövetregeneráció és fejlődési rekapituláció
Sérülésre válaszul az embrionális fejlődés során normálisan aktív gének újra kifejeződnek. Az őssejtek és a proliferatív sejtpopulációk bővülnek és differenciálódnak specializált szövetekké; a felnőtt ín azonban általában nem tud teljesen regenerálódni, gyakran visszamaradó degeneratív mátrixot hagyva maguk után. Ezzel szemben az újszülöttkori modellek nagyobb képességet mutatnak a funkcionális javításra, a szöveti szerveződés pedig hasonlít a fejlődési folyamatokra. Ezek az eredmények arra utalnak, hogy a regenerációs képesség a fejlődési programok újraképzésének képességétől függhet, amely tulajdonság a fiatalabb szervezetekben és bizonyos kísérleti modellekben erőteljesebbnek tűnik, mint a felnőtt emberi ín-gyógyulásban.
Az anyagtulajdonságok mechanikai igénybevételt tükröznek
Az inakat mechanikai funkciójuk szerint energiaraktározó vagy pozícionáló szerkezetekként lehet kategorizálni. Az energiatároló inak, mint például az Achilles-ín, elnyelik és visszaadják a mechanikai energiát a mozgásszervi hatékonyság növelése érdekében. A pozicionáló inak, mint például a tibialis anterior ín, elsősorban az ízületeket pozícionálják és megkönnyítik az olyan mozgásokat, mint például a járás közbeni lábtisztítás. Ezek a funkcionális különbségek a szerkezeti tulajdonságokban is tükröződnek: az energiatároló ín jellemzően nagyobb keresztmetszettel rendelkezik, ami kompenzálja az alacsonyabb anyagmerevséget, és lehetővé teszi a rugalmas energiatárolást. Az ugyanazon kinetikus láncon belüli ín eltérő mechanikai jellemzőkkel is rendelkezhet. Például a quadricepsz ín és a patella-ín egymás után működik, de eltérő merevségi tulajdonságokkal rendelkezik, a quadricepsz ín körülbelül kétszer kevésbé merev. Ez a különbség valószínűleg a mechanikai környezetüket tükrözi - a patella-ín csont-csont tapadása a patella-ín esetében versus a quadricepsz izom-csont rögzítése -, amely eltérő terhelési mintákat ír elő, és ezért befolyásolja az anyag igénybevételét. mechanikai terhelés az ín adaptációjára és az anyagigényt.
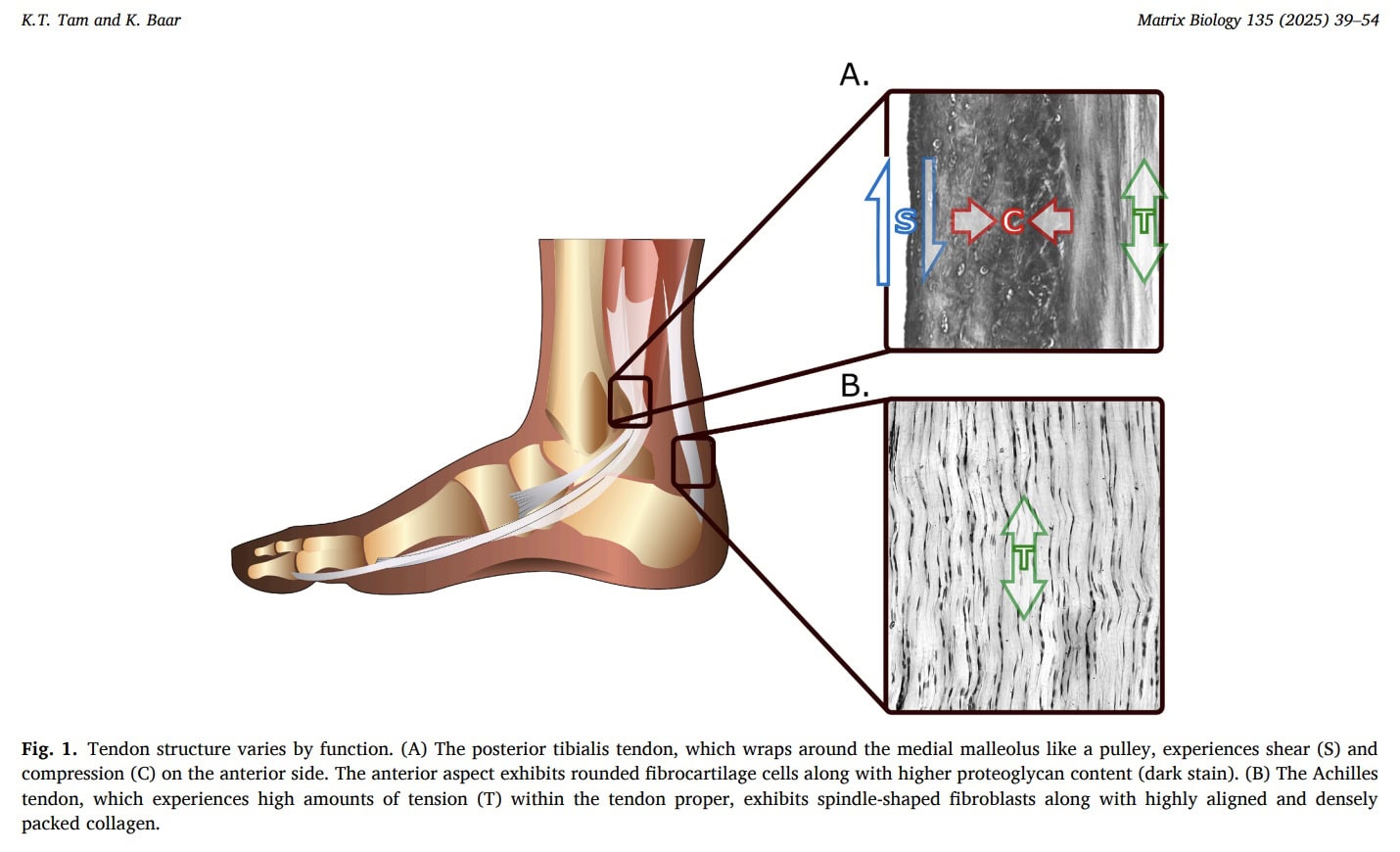
Kompresszió
A nyomóerők gyakran hatnak az ínkre, különösen ott, ahol azok csontos vagy retinás struktúrákat ölelnek körül. Állatmodelleken végzett kísérleti vizsgálatok azt mutatják, hogy a nyomóterhelés megszüntetése csökkenti az ín merevségét és megváltoztatja a szerkezeti adaptációt, ami utalás arra, hogy a nyomóterhelésnek kitett inak átalakulnak, hogy alkalmazkodjanak ehhez a mechanikai környezethez. Emberekben a komprimált ínrégiók gyakran mutatnak II-es típusú kollagénben gazdag fibrokartilaginás jellemzőket, amelyek a nyomóerőknek való ellenállásra specializálódtak.
Nyíró
A nyíróerők az inak, szalagok, izomok és a szomszédos szövetek közötti relatív csúszásból erednek. Az Achilles-ínban a differenciális csúszás a fasciculák között megkönnyíti az erőátvitelt, de az életkor előrehaladtával csökkenhet, ami hozzájárulhat a csökkent mozgástartományhoz és a károsodott erőeloszláshoz. A csúszóképesség csökkenése részben magyarázhatja az Achilles-ín szakadás nagyobb előfordulási gyakoriságát az idősebb egyéneknél. A kompressziós adaptációhoz hasonlóan a csökkent mechanikai terhelés is hozzájárulhat a degeneratív változásokhoz, a megnövekedett sérülési kockázathoz és a desadaptációhoz.
Specifikus erők hajtják a specifikus molekuláris programokat
A sejtsorsot és a szövet összetételt a mechanikai környezet erősen befolyásolja a mechanotranszdukciós útvonalakon keresztül, hangsúlyozva a következők fontosságát a mechanikai terhelés hatása az ín adaptációjára. A mechanikai erők biológiai és metabolikus adaptációkat indítanak el, amelyek szabályozzák a szövet szerkezetét és működését, bár az ín gyógyulását irányító specifikus útvonalak még nem teljesen ismertek. A következő szakaszok a különböző terhelési módok biomechanikai hatásait vizsgálják az ín adaptációjára és javulására.
Feszültség
A mechanikai környezet manipulációja, beleértve mechanikai terhelésközponti szerepet játszik az ín átalakításában és a funkcionális adaptációban. A húzóterhelés irányítja a szöveti átalakulást, de a kedvező és a potenciálisan káros terhelések közötti egyensúly továbbra is kritikus. A terhelési stratégiák erősebb biomechanikai megértése ezért elengedhetetlen az ín rehabilitációjának és adaptációjának optimalizálásához.
A szkleraxis (Scx) egy kulcsfontosságú transzkripciós faktor, amely részt vesz az ín fejlődésében és a kollagén szabályozásában. Az embriogenezis során az Scx elősegíti az I. típusú kollagén (COL1) szintézisét azáltal, hogy a Col1a1 gén szabályozó régióihoz kötődik. Expresszióját az izomaktivitás és a mechanikai terhelés befolyásolja. A felnőtt ínben azonban az Scx kevésbé tűnik lényegesnek az adaptív növekedéshez. Számos tenogén gén - köztük a Col1a1, a tenomodulin (Tnmd), a fibromodulin (Fmod) és a Mohawk (Mkx) - felszabályozódhat terhelés hatására anélkül, hogy az Scx expressziójában megfelelő változások következnének be. Ez arra utal, hogy az ín adaptációja az Scx-től függetlenül is bekövetkezhet, és hogy elsődleges szerepe inkább a korai fibrillaképződéshez, mint a későbbi fibrillanövekedéshez kapcsolódhat. Ezzel szemben az Mkx úgy tűnik, hogy hozzájárul a fibrillák megnagyobbodásához és éréséhez mechanikai stimulációra adott válaszként, ami alátámasztja az ínszerkezeti adaptációban betöltött szerepét.
A gyógyuló felnőtt ínszövetek gyakran mutatnak a fejlődési szövethez hasonló tulajdonságokat, beleértve a kis átmérőjű kollagénfibrillákat és az emelkedett Scx expressziót. Az embrionális fejlődéssel ellentétben azonban a gyógyulási mátrix gyakran nem érik szervezett, teherbíró szövetté. Az egyik magyarázat az, hogy a mechanikai jelek nem jutnak át megfelelően a heges mátrixon, ami a stressz leárnyékolásával összhangban lévő jelenség (amelyet alább tárgyalunk). A károsodott mechanikai jelátvitel csökkentheti a mechanoszenzitív útvonalak, például az Mkx aktiválódását, korlátozva a kollagén fibrillumok érését és hozzájárulva a mechanikailag rosszabb hegszövet kialakulásához.
Kompresszió
A kompressziós erők szabályozzák az ínsejtek differenciálódását és a mátrix összetételét. A kompressziónak kitett régiókban - mint például az enthesis és az íncsigolyák - gyakran alakulnak ki rostos-porcos jellegzetességek, amelyeket a porcmarkerek, köztük a Col2a1 és az aggrecan expressziója jellemez. Fejlődési szempontból az ínprogenitorok kezdetben együttesen expresszálják a Scx-et és a Sox9-et (egy kondrogén transzkripciós faktor), mielőtt szétválnának feszültségre adaptált ínsejtekre és kompresszióra adaptált fibrokartikuláris sejtekre. Kísérleti bizonyítékok azt mutatják, hogy a tartós kompresszió porcszerű szövetképződést indukálhat az ínban, míg a húzóterhelés elősegíti az ínspecifikus génexpressziót és elnyomja a kondrogén útvonalakat. Az Mkx hiányában a húzódás paradox módon kedvezhet a kondrogén gének expressziójának, ami ektopikus fibro-ízület kialakulásához vezet. Ezek az eredmények azt mutatják, hogy az ínsejtek multipotens potenciállal rendelkeznek, és hogy a mechanikai terhelés a feszültség- és kompresszióérzékeny transzkripciós programokon keresztül szabályozza a differenciálódást.
Nyírás
A lubricin és a hialuronsav fontos közvetítői az ínszalagok siklásának és a nyírási terhelésnek. Ugyanakkor biológiai szabályozásuk és a mechanikai terhelésre adott válaszuk továbbra sem eléggé jellemzett, ami korlátozza az ín patológiájában és adaptációjában játszott szerepük megértését.
Térbeli elrendezés
A kollagénszerveződés alapvető fontosságú az ín működéséhez, és erősen szabályozza a mechanikai feszültség. A fejlődés során a húzóerők a sejteket és a kollagénfibrillumokat speciális struktúrákon (fibripositorok) keresztül igazítják egymáshoz, így jön létre az egészséges ínkre jellemző párhuzamos architektúra. Még az acelluláris kollagénmátrixokban is a húzódás növelheti a fibrillumok igazodását és sűrűségét, és ezek a változások a terhelés megszüntetése után is perzisztensek lehetnek. A remodelling állandósága azonban a mátrix keresztkötésétől függ, ami öregedő vagy metabolikusan megváltozott szövetekben, például cukorbetegségben, csökkentheti az alkalmazkodóképességet. A húzóterhelés növeli a kollagén degradációval szembeni ellenállást is, és aktiválja a fibrillumok érését támogató biokémiai útvonalakat (beleértve az Mkx-et). Ín adaptációja tehát a passzív mechanikai igazodás és az aktív sejtszintű jelátvitel kölcsönhatását tükrözi, válaszul a mechanikai igénybevételre. mechanikai terhelésre, egy olyan folyamat, amely a szerkezeti átalakulást és a funkcionális optimalizálást irányítja.
A hiányzó és aberráns erők szerepet játszanak az ín- és szalagdegenerációban
A gyógyuló ín gyakran hasonlít az éretlen vagy embrionális szövetre, emelkedett Scx-expressziót, fokozott fibrillogén kollagéneket (III, V, XI), kis átmérőjű kollagénfibrillákat, nagyfokú sejtszintűséget, érrendszeri vaszkularizációt és Scx+/Sox9+ progenitorok jelenlétét mutatják. Ezek a jellemzők arra utalnak, hogy a sérült ín reaktivál egy fejlődési programot, de nem halad a teljes mechanikai érés felé, valószínűleg a megváltozott mechanikai jelátvitel miatt. A mechanikai terhelés elengedhetetlen a megfelelő ín-szabályozáshoz: a bénulás vagy a terhelés hiánya csökkenti a kulcsfontosságú mechanoszenzitív transzkripciós faktorokat, például az Egr1-et, és megzavarja a TGF-β által közvetített Scx jelátvitelt, ami okoz károsodást a regenerációs képességben. A húzóterhelés elősegíti az ínspecifikus gének kifejeződését, miközben elnyomja a porcgéneket, míg a kompresszió vagy a tehermentesítés a kondrogén vagy degeneratív fenotípusok felé tolja el az egyensúlyt. Bár a kollagén III-at általában a hegszövethez társítják, a regenerációs modellekből származó bizonyítékok azt mutatják, hogy korai felszabályozása a normális javulás része. A perzisztens emelkedés, különösen terheletlen állapotban, inkább a sikertelen érést tükrözi, mintsem a degeneráció okát. Még minimális mechanikai húzódás is elegendő a mátrixgének expressziójának szabályozásához és a mechanikai felépülés javításához, ami rávilágít az ínsejtek terhelési környezetükre való rendkívüli szenzitivitásukra. Ezek az eredmények együttesen azt sugallják, hogy mind a hiányzó, mind az aberráns mechanikai erők megszakítják a korai javítómátrixból az érett, mechanikailag kompetens ín felé vezető normális progressziót.
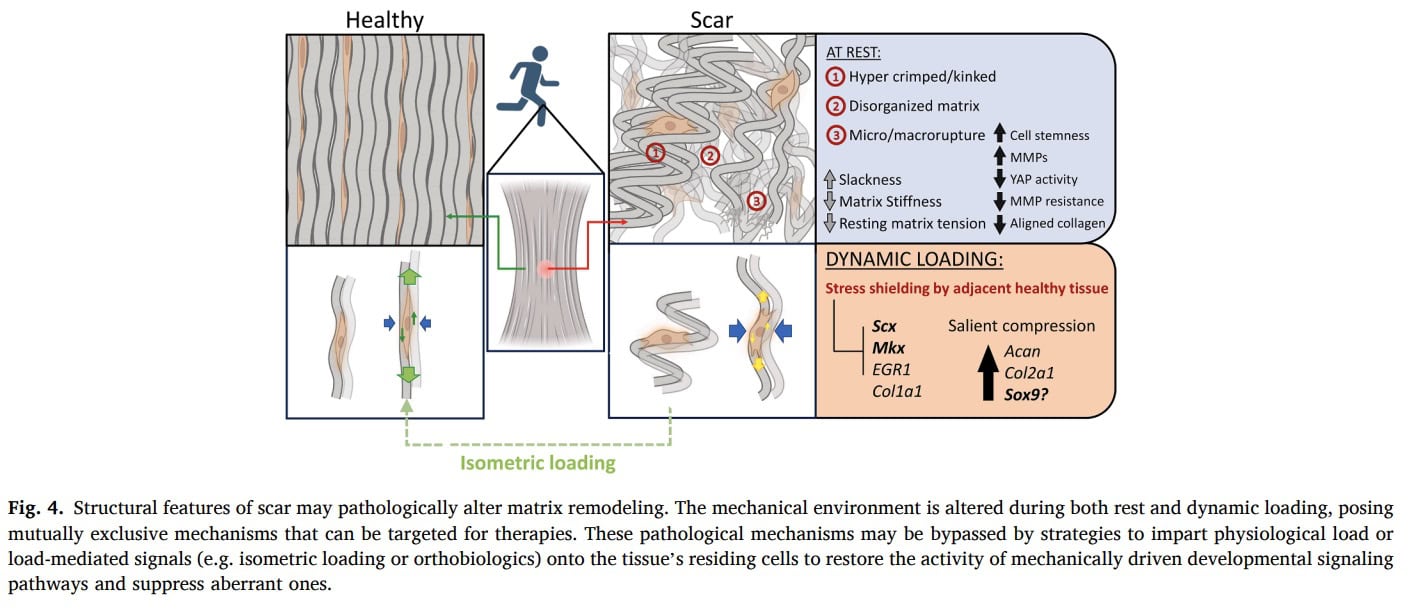
Stressz elleni védelem
Íngyulladás előrehaladtával a degeneratív ínszakaszok szimptomatikusak lehetnek, és stresszpajzsosodásnak lehetnek kitéve. Mechanikai terheléskor az ín merevebb és egészségesebb részei előnyben részesítik a terhelést, míg a rugalmasabb degeneratív régiók nem terhelhetők. Ez a biomechanikai jelenség tovább csökkenti a beteg szövet mechanikai stimulációját, és hozzájárulhat a használaton kívüliséghez és a károsodott átalakuláshoz. Mivel a degeneratív rész kevés effektív terhelést kap, az ín adaptációs képessége a mechanikai terhelésen keresztül mechanikai terhelés csökken.
Az ín viszkoelasztikus viselkedést mutat, ami terápiásan kihasználható. Két kulcsfontosságú tulajdonság a feszültségrelaxáció - a belső feszültség fokozatos csökkenése tartós nyújtás során - és a kúszás, a szövet időfüggő deformációja állandó terhelés alatt. Ezek a tulajdonságok arra utalnak, hogy a kontrollált, tartós terhelési stratégiák elősegíthetik a degeneratív régiók mechanikai stimulációját a stressz leárnyékolása ellenére.
Az izometrikus összehúzódások értékes terhelési módot jelenthetnek. Kísérleti modellek kimutatták, hogy az izometrikus terhelés felszabályozhatja a tenogén gének expresszióját. A hosszan tartó izometrikus összehúzódások stresszrelaxációt idézhetnek elő az egészségesebb ínterületeken, miközben lehetővé teszik a kúszást és a mechanikai húzódást a degeneratív területeken. Ez megkönnyítheti a terhelés átvitelét a heges szövetre, és potenciálisan támogathatja a biológiai és strukturális adaptációt.
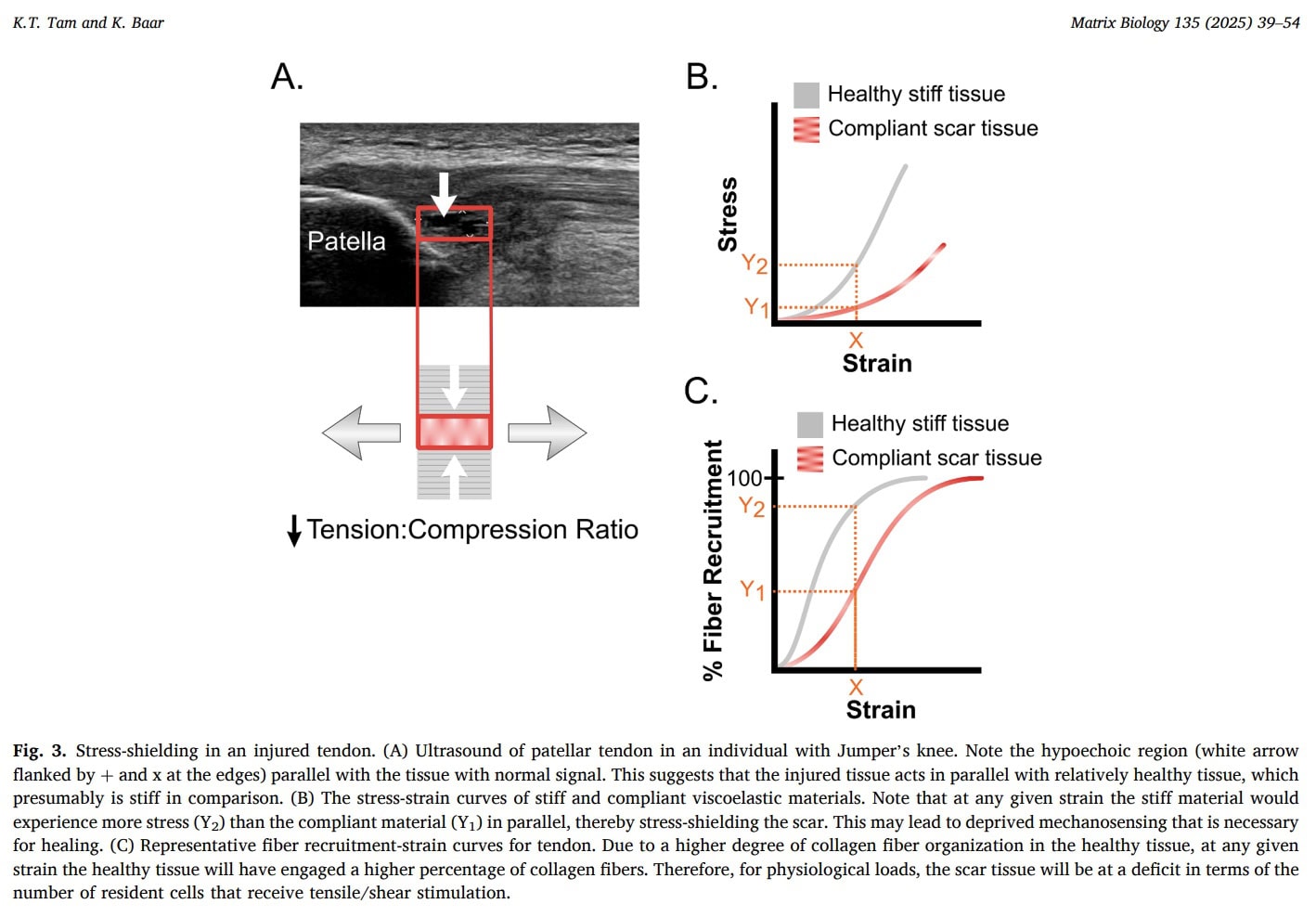
Kérdések és gondolatok
Tam et al. (2025) azt javasolják, hogy íngyulladásban az engedékeny hegszövet párhuzamosan ülhet a merevebb egészséges ínnal, és mechanikailag "feszültség-árnyékolttá" válhat, ami azt jelenti, hogy normál fiziológiai húzódási szintek mellett a hegben lévő kevesebb kollagénrost és rezidens sejt valójában húzófeszültséget tapasztal. Mivel a kulcsfontosságú tenogenetikai szabályozók terhelésérzékenyek, az elégtelen stresszátvitel megakadályozhatja a heg érését, és ehelyett az éretlen vagy fibrokartilág-szerű fenotípus fennmaradásának kedvezhet. A klinikai gyakorlat számára ez a modell alátámasztja a gondosan adagolt mechanikai terhelés indokoltságát a hosszan tartó tehermentesítés helyett: a teljes stresszmegvonás bizonyítottan okoz károsodást a tenogén génexpresszióban és a mechanikai felépülésben. A szerzők továbbá azt sugallják, hogy a viszkoelasztikus kúszást lehetővé tevő tartós terhelés (pl. izometrikus összehúzódások) segíthet a feszültségnek a hegbe történő továbbításában és a tenogén útvonalak aktiválásában, míg a nem megfelelő vagy hiányzó terhelés állandósíthatja a degenerációt. Fontos azonban hangsúlyozni, hogy bár ez a mechanobiológiai keretrendszer plauzibilis magyarázatot ad arra, hogy miért lehet előnyös a kontrollált terhelés, és miért lehet helytelen a mindenféle terheléstől való félelem, közvetlen klinikai bizonyítékot arra vonatkozóan, hogy az egyes terhelési stratégiák "legyőzik" a stresszpajzsot az emberekben, ebben a tanulmányban még nem találtak.
Az izometrikus terhelés ígéretes módszere az ín rehabilitációjának, de az optimális edzési paraméterek továbbra is bizonytalanok. Ebben az esettanulmánybanegy kombinált izometrikus terheléses programot és étrend-kiegészítő protokollt alkalmaztak egy krónikus patelláris ínhüvelygyulladásban szenvedő sportoló esetében. A diétás stratégia 15 g zselatinból és 225 mg C-vitaminból állt, amelyet körülbelül egy órával az edzések előtt fogyasztottak el, a kollagénszintézis támogatására törekedve.
Az izometrikus gyakorlat az ín középső terhelését célozta, mind nyitott láncú (lábnyújtás és lábprés), mind zárt láncú (spanyol guggolás) gyakorlatokkal. Az izometrikus tartásokat kezdetben 10 másodpercig írták elő, és fokozatosan 5 másodperces lépésekkel növelték a maximális 30 másodpercig. Az edzés mennyisége egy-három, 2-4 ismétlésből álló sorozatból állt, az egy ismétléses maximum (1 RM) 80%-át meghaladó intenzitással, amelyet havonta újraszámoltak. Az ülések körülbelül 10 percig tartottak, a tartási időtartamokat azon bizonyítékok alapján választották ki, amelyek azt mutatják, hogy a patella-ín feszültsége nagyjából 60%-kal csökken 30 másodpercen belül a tartós összehúzódás után, és csak kis mértékben ezt követően.
A 18 hónapos beavatkozás során a terhelés és a tartás időtartamának fokozatos növelése az erő javulásával járt együtt minden ellenállással végzett feladatban (lábnyújtás, lábprés és spanyol guggolás tartása). A mágneses rezonancia képalkotás (MRI) a kiindulási, 12 hónapos és 18 hónapos vizsgálat során az ínreaktivitás csökkenését, az ín átmérőjének növekedését a középső állományban és a vastagság csökkenését a proximális tapadásnél mutatta, ami összhangban van a strukturális átalakulással. A sportoló fokozatos fájdalomcsökkenésről számolt be, és a 18 hónapos utánkövetéskor fájdalommentes volt.
Ezek a megfigyelések arra utalnak, hogy az izometrikus edzés, különösen ha kollagénszintézist támogató táplálkozási stratégiákkal kombinálják, elősegítheti az ín adaptációját és a tünetek javulását. Bizonyítékok azonban továbbra is kísérleti tanulmányokra és elszigetelt esetjelentésekre korlátozódnak. Nagyobb, kontrollált vizsgálatokra van szükség az izometrikus protokollok hatékonyságának és optimális paramétereinek meghatározásához. Ezenkívül az ín tulajdonságai az anatómiai elhelyezkedés, a keresztmetszeti terület és a mechanikai környezet függvényében változnak, ami befolyásolhatja a viszkoelasztikus viselkedést és a megfelelő terhelési stratégiákat. Amint azt ebben az áttekintésben is hangsúlyozták, a sikeres rehabilitáció valószínűleg az alulterhelés és a túlzott terhelés közötti megfelelő egyensúly elérésétől függ, hangsúlyozva, hogy megbízható klinikai eszközökre van szükség az ínadaptáció monitorozásához. a mechanikai terhelés nyomon követése az ín adaptációjához.
Beszélj hozzám szakértőként
Bár az elbeszélő áttekintéseknek ki vannak téve az olyan inherens torzításoknak, mint a szelekciós torzítás, ez az áttekintés alapvető biológiai kontextust biztosít, amely segíthet a gyógytornászoknak jobban megérteni az ínszerkezetet és a mechanobiológiát az íngyulladás kezelésében. A genetikai szabályozás, a transzkripciós útvonalak, az aminosavdinamika és a fehérje remodelling ismerete hozzájárul az ín gyógyulásának és adaptációjának mélyebb megértéséhez, ami a rehabilitációs stratégiákhoz is hozzájárulhat. A legtöbb mechanisztikus bizonyíték azonban állatmodellekből származik, és a közvetlen extrapoláció a humán ín-patológia területére korlátozott.
Míg a bizonyítékbázis megerősítéséhez fejlettebb klinikai vizsgálatokra van szükség, e sorozat következő cikke egy 2022-es tanulmány adatait vizsgálja, amely egy olyan nagy terhelésű edzésprotokollt vizsgál, amelynek célja az ín keresztmetszeti területének növelése, valamint a fájdalom és a funkció javítása Achilles tendinopathiaban szenvedő betegeknél.
Főbb üzenetek
- Az inak élő, adaptív szövetek. A mechanikai terhelésre sejtszintű jelátvitel és mátrix átalakítás révén reagálnak. A mechanikai ingerek irányítják a szerkezeti adaptációt - az ín nem inaktív struktúrák.
- A biomechanikai terhelés elengedhetetlen az adaptációhoz. A megfelelő mechanikai terhelés elősegíti az inak egészségét és átalakulását, támogatva a funkcionális felépülést és a strukturális javulást az alábbiak révén az ín adaptációjának mechanikai terhelése.
- A stressz leárnyékolása korlátozza az adaptációt. A degeneratív ínszakaszok tehermentesíthetők, amikor az egészségesebb szövet viseli a mechanikai terhelés nagy részét. Ez csökkenti a hatékony mechanikai stimulációt és akadályozhatja a felépülést.
- A rehabilitációnak le kell küzdenie a stresszárnyékolást. A terhelési stratégiáknak arra kell törekedniük, hogy mechanikai erőket közvetítsenek a degeneratív szövetek felé, ugyanakkor elkerüljék a túlzott húzódást. A viszkoelasztikus tulajdonságok (feszültségrelaxáció és kúszás) biomechanikai alapot biztosítanak a kontrollált, terápiás terheléshez.
- A kiegyensúlyozott terhelés kulcsfontosságú. Az inaknak elegendő mechanikai ingerre van szükségük az adaptációhoz, de sérülékenyek az alulterhelésre (ami a használaton kívüliséget állandósítja) és a túlterhelésre (ami súlyosbíthatja a tüneteket). Az egyénre szabott, progresszív terhelés elengedhetetlen.
- Klinikai következmények a gyógytornára nézve. A rehabilitációnak olyan mérhető és progresszív terhelési stratégiákra kell összpontosítania, amelyek helyreállítják a beteg szövetek mechanikai stimulációját és kihasználják az ínok alkalmazkodóképességét.
- Következő lépések. A következő cikk ezeket a biomechanikai elveket klinikai stratégiákra fordítja le, áttekintve a nagy terhelésű edzésprotokollokat és gyakorlati megközelítéseket az ín adaptációjának, a fájdalomcsökkentésnek és a funkcionális felépülésnek az íngyulladás optimalizálására.
Ez az erőforrás A Physiotutors-tól származó forrás további szempontokat nyújt az inak biológiájáról és mechanobiológiájáról, klinikailag releváns betekintést nyújtva az inak működésébe és adaptációjába.
Referencia
A VMO ÉS A QUADRICEPS SZEREPE A PFP ESETÉBEN
Nézd meg ezt a INGYENES, 2 RÉSZBŐL ÁLLÓ VIDEÓ ELŐADÁST Claire Robertson térdfájdalom szakértőtől, aki elemzi a témával kapcsolatos szakirodalmat és annak klinikai gyakorlatra gyakorolt hatását.