Effekten af mekanisk belastning på senetilpasning - biologisk baggrund for præcise øvelsesterapiinterventioner
Introduktion
På trods af fremskridt i vores forståelse af tendinopatiens patogenese er resultaterne efter traditionelle konservative og medicinske interventioner fortsat inkonsekvente, og mange patienter oplever vedvarende smerter og funktionsbegrænsninger. Den meget citerede kontinuumsmodel foreslået af Jill Cook antyder, at den degenerative del af en sene er strukturelt irreversibel. Nye strukturelle og mekanobiologiske beviser udfordrer imidlertid denne antagelse og indikerer, at senevæv kan bevare en større kapacitet til tilpasning og omdannelse end tidligere antaget.
Denne gennemgang udforsker indflydelsen af mekanisk belastning på senetilpasning og de biologiske mekanismer, der ligger til grund for degeneration, med særligt fokus på cellulær signalering, matrixombygning og mekanotransduktionsveje. Ved at integrere de seneste eksperimentelle resultater sigter den mod at skabe en biologisk funderet ramme for at informere om træningsrecepter til behandling af tendinopati. Denne teoretiske syntese tjener som grundlag for en kommende gennemgang, der undersøger træningsstrategier med høj belastning og introducerer en ny belastningsprotokol for tendinopati til klinisk anvendelse.
Metoder
Denne narrative gennemgang sammenfatter resultater fra flere eksperimentelle studier, der overvejende er udført i dyremodeller.
Resultater
Biologisk grundlag for seners opbygning
Type I-kollagen (COL1/Col1a1) er det vigtigste strukturelle protein i sene- og ledbåndsvæv og giver trækstyrke. Efter en skade øges kollagensyntesen, men matrixaflejringen i den proliferative fase er ofte uorganiseret. Mens sunde sener har kollagenfibriller, der er rettet ind parallelt med de mekaniske kræfter, indeholder patologiske sener mindre, mindre tværbundne og uorganiserede fibriller. Selvom type I-kollagen giver bedre mekanisk modstand end type III-kollagen, indeholder helende sener ofte en højere andel af type III-kollagen. Matrix metalloproteinaser (MMP'er), enzymer, der er ansvarlige for kollagennedbrydning, er samtidig aktive under vævsreformering.
Skadede sener hos voksne bliver typisk stærkt cellulære og udvikler en uorganiseret kollagenmatrix, der er karakteriseret ved fibriller med lille diameter, hvilket resulterer i en degenerativ vævsfænotype.
Vævsregenerering og udviklingsmæssig rekapitulation
Som reaktion på skader genudtrykkes gener, der normalt er aktive under embryonaludviklingen. Stam- og proliferative cellepopulationer udvides og differentieres til specialiseret væv; men voksne sener kan generelt ikke regenereres fuldt ud og efterlader ofte en resterende degenerativ matrix. I modsætning hertil viser neonatale modeller en større kapacitet til funktionel reparation, hvor vævsorganisationen ligner udviklingsprocesser. Disse resultater tyder på, at regenerativ kapacitet kan afhænge af evnen til at rekapitulere udviklingsprogrammer, et træk, der virker mere robust i yngre organismer og visse eksperimentelle modeller end i senetilheling hos voksne mennesker.
Materialeegenskaber afspejler mekaniske krav
Sener kan kategoriseres i henhold til deres mekaniske funktion som enten energilagrende eller positionelle strukturer. Energilagrende sener, som f.eks. akillessenen, absorberer og returnerer mekanisk energi for at forbedre bevægeapparatets effektivitet. Positionelle sener, eksemplificeret ved tibialis anterior-senen, positionerer primært leddene og letter bevægelser som f.eks. fodafstand under gang. Disse funktionelle forskelle afspejles i de strukturelle egenskaber: Energilagrende sener har typisk et større tværsnitsareal, hvilket kompenserer for lavere materialestivhed for at muliggøre elastisk energilagring. Sener inden for samme kinetiske kæde kan også have forskellige mekaniske egenskaber. For eksempel fungerer quadriceps-senen og patellasenen i serie, men har forskellige stivhedsegenskaber, hvor quadriceps-senen er cirka to gange mindre stiv. Denne forskel afspejler sandsynligvis deres mekaniske miljøer - knogle-til-knogle-insertion for patellarsenen versus muskel-til-knogle-tilhæftning for quadriceps-senen - som påfører forskellige belastningsmønstre og derfor påvirker mekanisk belastning på senetilpasning og materialekrav.
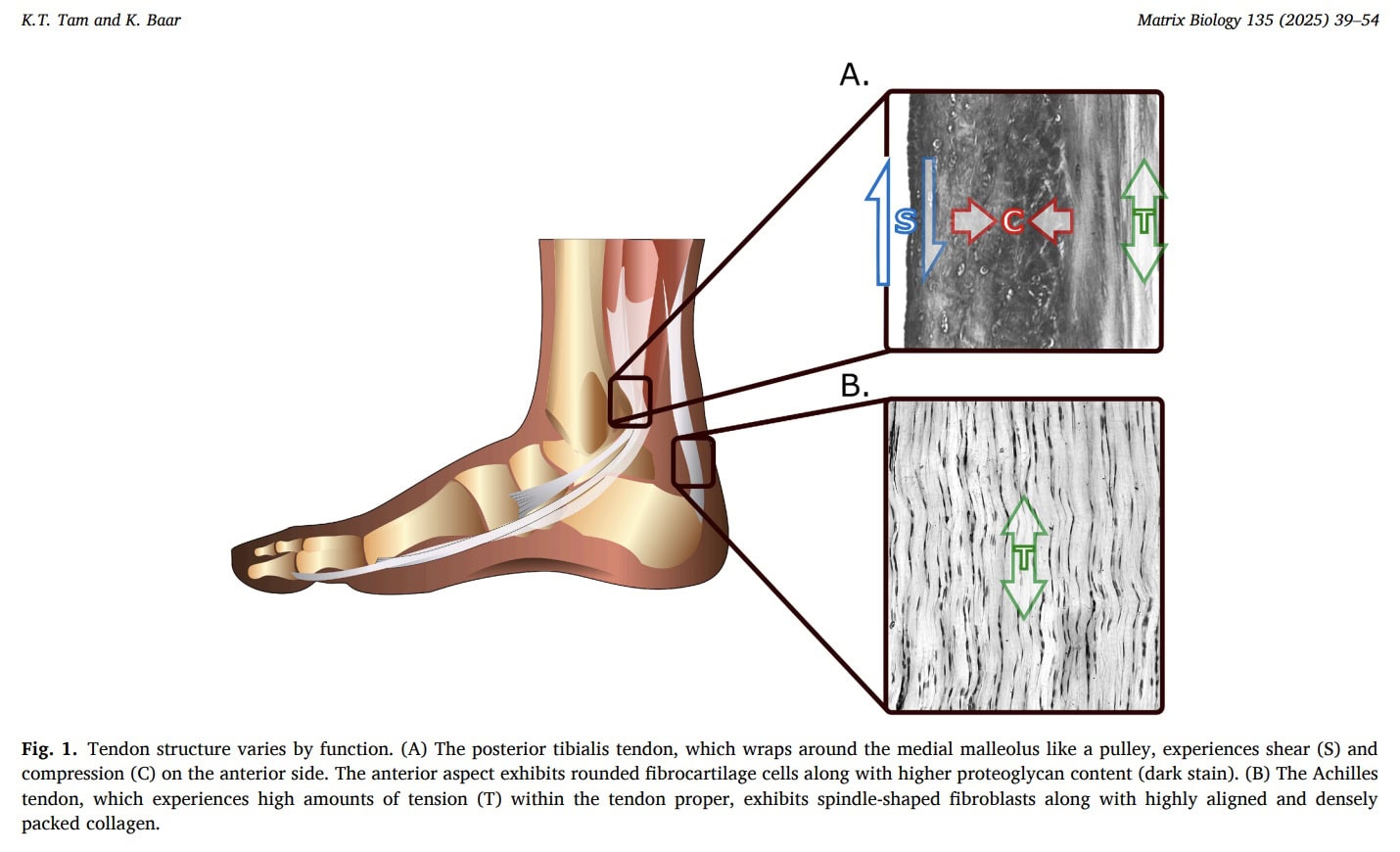
Kompression
Kompressionskræfter virker ofte på sener, især hvor de vikles rundt om knogler eller retinakulære strukturer. Eksperimentelle studier i dyremodeller viser, at fjernelse af trykbelastning reducerer senens stivhed og ændrer den strukturelle tilpasning, hvilket tyder på, at sener, der udsættes for kompression, ombygges for at tilpasse sig dette mekaniske miljø. Hos mennesker udviser komprimerede seneområder ofte fibrokartilaginøse træk, der er rige på type II-kollagen, der er specialiseret til at modstå trykkræfter.
Shear
Forskydningskræfter opstår ved relativ glidning mellem sener, ledbånd, muskler og tilstødende væv. I akillessenen letter differentiel glidning mellem fasciklerne kraftoverførsel, men kan mindskes med alderen, hvilket potentielt bidrager til reduceret bevægelsesområde og forringet kraftfordeling. Dette fald i glideevne kan til dels forklare den højere forekomst af akillessenerupturer hos ældre. Ligesom ved kompressiv tilpasning kan reduceret mekanisk belastning bidrage til degenerative forandringer, øget skadesrisiko og desadaptation.
Specifikke kræfter driver specifikke molekylære programmer
Celleskæbne og vævssammensætning er stærkt påvirket af det mekaniske miljø gennem mekanotransduktionsveje, hvilket understreger betydningen af mekanisk belastning på senetilpasning. Mekaniske kræfter igangsætter biologiske og metaboliske tilpasninger, der regulerer vævets struktur og funktion, selvom de specifikke veje, der styrer seneheling, stadig er ufuldstændigt forstået. De følgende afsnit undersøger de biomekaniske virkninger af forskellige belastningsmodaliteter på senetilpasning og -reparation.
Spænding
Manipulation af det mekaniske miljø, herunder mekanisk belastninger central for seneombygning og funktionel tilpasning. Trækbelastning driver vævsmodellering, men balancen mellem gavnlige og potentielt skadelige belastninger er stadig afgørende. En stærkere biomekanisk forståelse af belastningsstrategier er derfor afgørende for at optimere rehabilitering og tilpasning af sener.
Scleraxis (Scx) er en vigtig transkriptionsfaktor, der er involveret i seneudvikling og kollagenregulering. Under embryogenesen fremmer Scx syntesen af type I-kollagen (COL1) ved at binde sig til regulerende regioner i Col1a1-genet. Dens udtryk påvirkes af muskelaktivitet og mekanisk belastning. I voksne sener synes Scx dog at være mindre vigtig for den adaptive vækst. Flere tenogene gener - herunder Col1a1, tenomodulin (Tnmd), fibromodulin (Fmod) og Mohawk (Mkx) - kan opreguleres som reaktion på belastning uden tilsvarende ændringer i Scx-ekspressionen. Dette tyder på, at senetilpasning kan ske uafhængigt af Scx, og at dens primære rolle kan være relateret til tidlig fibrildannelse snarere end efterfølgende fibrilvækst. I modsætning hertil ser Mkx ud til at bidrage til fibrilforstørrelse og modning som reaktion på mekanisk stimulering, hvilket understøtter dens rolle i senens strukturelle tilpasning.
Helende voksne sener udviser ofte træk, der ligner udviklingsvæv, herunder kollagenfibriller med lille diameter og forhøjet Scx-ekspression. Men i modsætning til den embryonale udvikling modnes helingsmatrixen ofte ikke til organiseret, belastningsbærende væv. En forklaring er, at mekaniske signaler måske ikke transmitteres tilstrækkeligt gennem den arrede matrix, et fænomen, der er i overensstemmelse med stressafskærmning (diskuteres yderligere nedenfor). Nedsat mekanisk signalering kan reducere aktiveringen af mekanosensitive veje som Mkx, hvilket begrænser modningen af kollagenfibriller og bidrager til dannelsen af mekanisk inferiørt arvæv.
Kompression
Kompressionskræfter regulerer senecelledifferentiering og matrixsammensætning. Områder, der udsættes for kompression - såsom enthesis og seneskiver - udvikler ofte fibrocartilaginøse træk, der er karakteriseret ved udtryk af bruskmarkører, herunder Col2a1 og aggrecan. Udviklingsmæssigt udtrykker seneforstadier oprindeligt Scx og Sox9 (en kondrogen transkriptionsfaktor), før de adskilles i spændingstilpassede seneceller og kompressionstilpassede fibrocartilage-celler. Eksperimentelle beviser viser, at vedvarende kompression kan fremkalde brusklignende vævsdannelse i senen, mens trækbelastning fremmer senespecifik genekspression og undertrykker kondrogene veje. I fravær af Mkx kan trækbelastning paradoksalt nok favorisere kondrogen genekspression, hvilket fører til ektopisk dannelse af fibrobrusk. Disse resultater tyder på, at seneceller har et multipotent potentiale, og at mekanisk belastning styrer differentieringen gennem spændings- og kompressionsfølsomme transkriptionsprogrammer.
Klipning
Lubricin og hyaluronsyre er vigtige formidlere af senefasciklens glidning og forskydningsmodstand. Men deres biologiske regulering og respons på mekanisk belastning er stadig utilstrækkeligt karakteriseret, hvilket begrænser forståelsen af deres rolle i senepatologi og -tilpasning.
Rumlig placering
Organiseringen af kollagen er afgørende for senens funktion og er stærkt reguleret af mekanisk spænding. Under udviklingen justerer trækkræfter celler og kollagenfibriller gennem specialiserede strukturer (fibripositorier), hvilket giver den parallelle arkitektur, der er karakteristisk for sunde sener. Selv i acellulære kollagenmatricer kan trækstamme øge fibrillernes tilpasning og tæthed, og disse ændringer kan fortsætte efter aflastning. Ombygningens varighed afhænger dog af matrixens tværbinding, som kan reducere tilpasningsevnen i aldrende eller metabolisk ændret væv, som f.eks. diabetes. Trækbelastning øger også modstanden mod kollagennedbrydning og aktiverer biokemiske veje (herunder Mkx), der understøtter modning af fibriller. Senetilpasning afspejler derfor samspillet mellem passiv mekanisk justering og aktiv cellulær signalering som reaktion på mekanisk belastningen proces, der styrer strukturel ombygning og funktionel optimering.
Fraværende og afvigende kræfter spiller en rolle i sene- og ledbåndsdegeneration
Helende sener ligner ofte umodent eller embryonalt væv med forhøjet Scx-ekspression, øgede fibrillogene kollagener (III, V, XI), kollagenfibriller med lille diameter, høj cellularitet, vaskularisering og tilstedeværelse af Scx+/Sox9+ progenitorer. Disse træk tyder på, at den skadede sene genaktiverer et udviklingsprogram, men ikke udvikler sig til fuld mekanisk modning, sandsynligvis på grund af ændret mekanisk signalering. Mekanisk belastning er afgørende for korrekt regulering af senegener: Lammelse eller aflastning reducerer vigtige mekanosensitive transkriptionsfaktorer som Egr1 og forstyrrer TGF-β-medieret Scx-signalering, hvilket forringer den regenerative kapacitet. Trækbelastning fremmer senespecifik genekspression, mens bruskgener undertrykkes, mens kompression eller aflastning forskyder balancen i retning af kondrogene eller degenerative fænotyper. Selvom kollagen III ofte forbindes med arvæv, viser beviser fra regenerative modeller, at dets tidlige opregulering er en del af den normale reparation. Vedvarende forhøjelse, især under aflastningsforhold, afspejler mislykket modning snarere end årsagen til degeneration. Selv en minimal mekanisk belastning er tilstrækkelig til at regulere matrixgenekspressionen og forbedre den mekaniske genopretning, hvilket understreger senecellernes ekstreme følsomhed over for deres belastningsmiljø. Tilsammen tyder disse resultater på, at både fraværende og afvigende mekaniske kræfter forstyrrer den normale udvikling fra en tidlig reparationsmatrix til en moden, mekanisk kompetent sene.
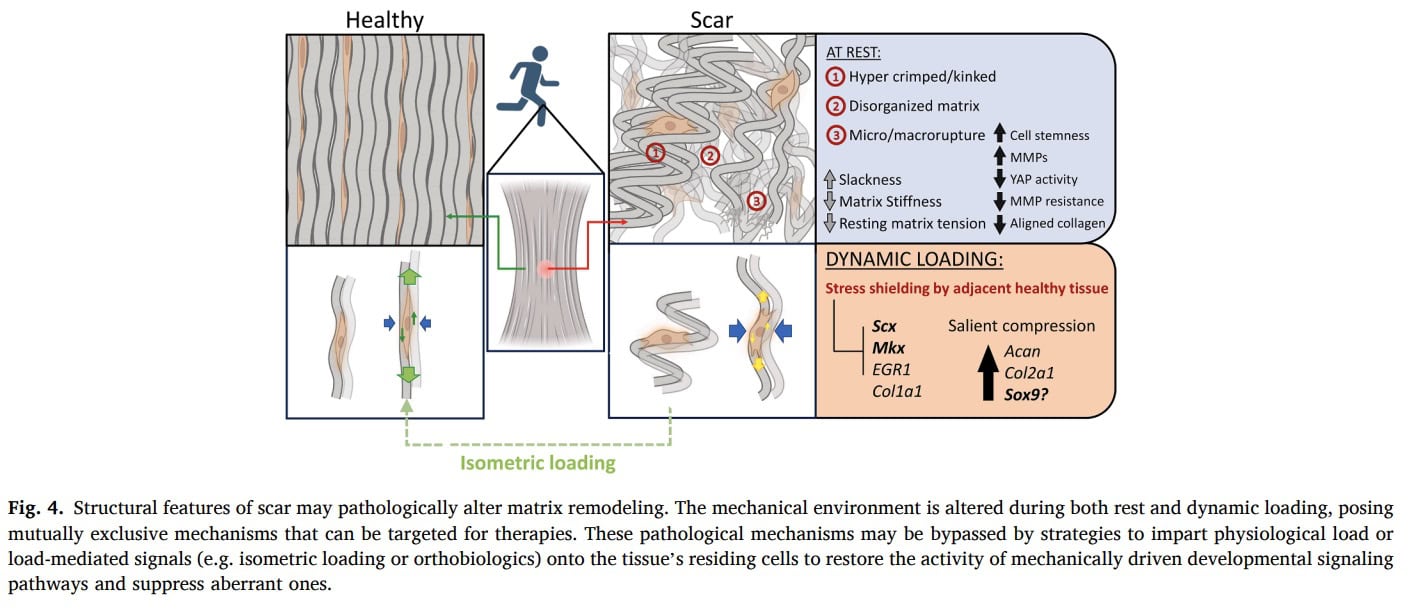
Afskærmning mod stress
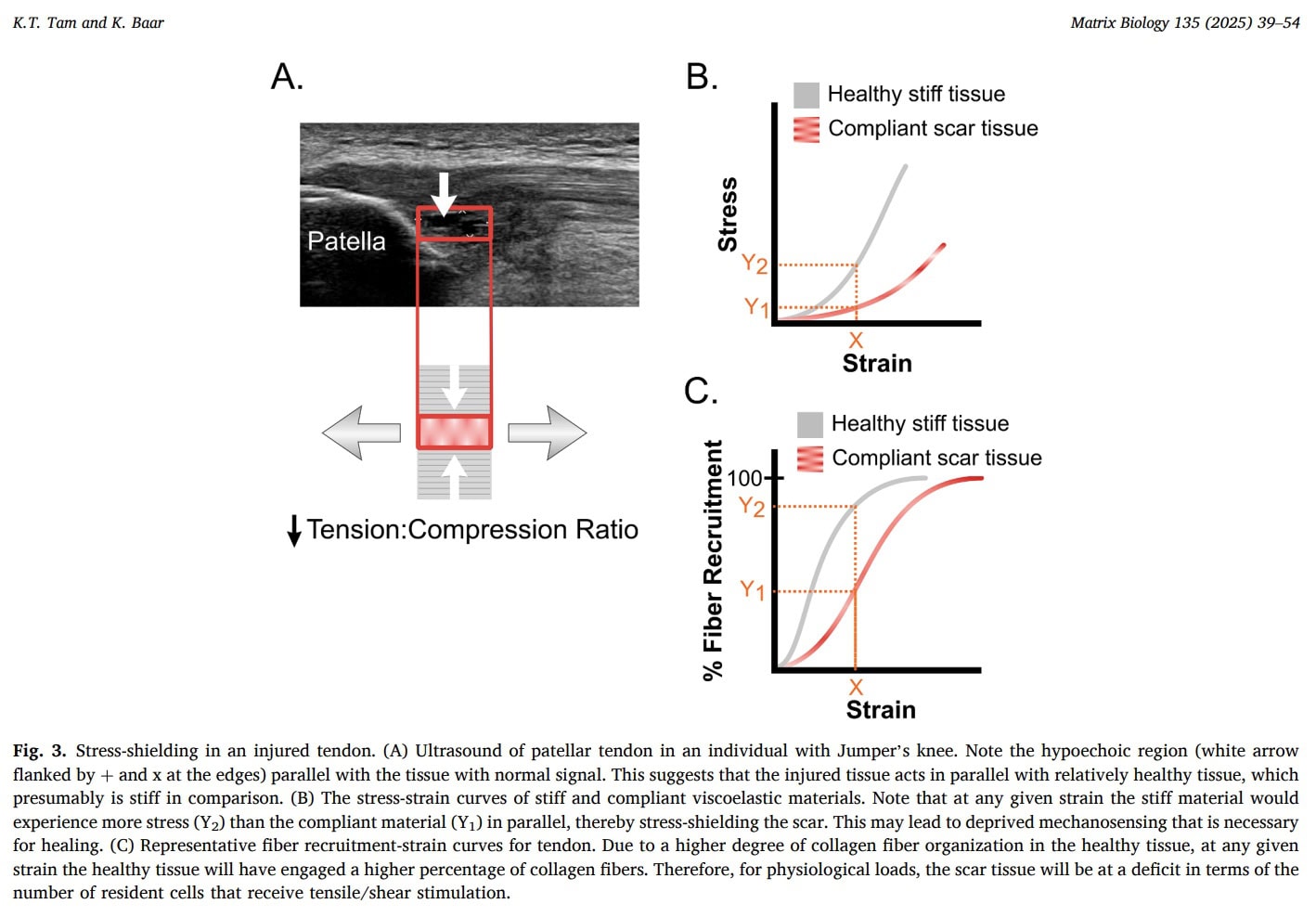
Efterhånden som tendinopatien skrider frem, kan de degenerative seneregioner blive symptomatiske og udsat for stressafskærmning. Når senen udsættes for mekanisk belastning, vil de stivere og sundere dele af senen fortrinsvis bære belastningen, mens de mere eftergivelige degenerative områder ikke belastes. Dette biomekaniske fænomen reducerer yderligere den mekaniske stimulering af det syge væv og kan bidrage til manglende brug og nedsat remodellering. Fordi den degenerative del modtager lidt effektiv belastning, er dens kapacitet til seneadaptation gennem mekanisk belastning reduceret.
Sener udviser viskoelastisk adfærd, som kan udnyttes terapeutisk. To nøgleegenskaber er stressrelaksation - det gradvise fald i indre spænding under et vedvarende stræk - og krybning, den tidsafhængige deformation af væv under konstant stress. Disse egenskaber tyder på, at kontrollerede, vedvarende belastningsstrategier kan fremme mekanisk stimulering af degenerative områder på trods af stressafskærmning.
Isometriske sammentrækninger kan udgøre en værdifuld belastningsmodalitet. Eksperimentelle modeller har vist, at isometrisk belastning kan opregulere det tenogene genudtryk. Langvarige isometriske sammentrækninger kan fremkalde stressafslapning i sundere seneområder, mens de tillader krybning og mekanisk belastning i degenerative områder. Det kan lette overførslen af belastning til det arrede væv og potentielt understøtte biologisk og strukturel tilpasning.
Spørgsmål og tanker
Tam et al. (2025) foreslår, at ved tendinopati kan eftergivende arvæv sidde parallelt med stivere sund sene og blive mekanisk "stressafskærmet", hvilket betyder, at færre kollagenfibre og celler i arret faktisk oplever trækstress ved normale fysiologiske belastningsniveauer. Da vigtige tenogene regulatorer er belastningsfølsomme, kan utilstrækkelig stresstransmission forhindre armodning og i stedet fremme persistensen af en umoden eller fibrocartilage-lignende fænotype. I klinisk praksis understøtter denne model begrundelsen for omhyggeligt doseret mekanisk belastning i stedet for langvarig aflastning: Det har vist sig, at fuldstændig stressdeprivation forringer det tenogene genudtryk og den mekaniske genopretning. Forfatterne foreslår desuden, at vedvarende belastning, der tillader viskoelastisk krybning (f.eks. isometriske sammentrækninger), kan hjælpe med at overføre spændinger til arret og aktivere tenogene veje, mens uhensigtsmæssig eller fraværende belastning kan forevige degeneration. Det er dog vigtigt at understrege, at selv om denne mekanobiologiske ramme giver en plausibel forklaring på, hvorfor kontrolleret belastning kan være gavnlig, og hvorfor frygt for al belastning kan være malplaceret, er direkte klinisk bevis for, at specifikke belastningsstrategier "overvinder" stressafskærmning hos mennesker, endnu ikke etableret i denne artikel.
Isometrisk belastning er en lovende metode til senerehabilitering, men de optimale træningsparametre er stadig usikre. I dette casestudieblev et kombineret isometrisk belastningsprogram og kosttilskudsprotokol anvendt på en atlet med kronisk patellar tendinopati. Koststrategien bestod af 15 g gelatine med 225 mg C-vitamin, der blev indtaget ca. en time før træningssessioner, med det formål at støtte kollagensyntesen.
Det isometriske træningsprogram var rettet mod senebelastning i mellemområdet ved hjælp af øvelser med både åben kæde (benforlængelse og benpres) og lukket kæde (spansk squat). Isometriske hold blev oprindeligt ordineret i 10 sekunder og blev gradvist øget med 5 sekunders intervaller til maksimalt 30 sekunder. Træningsvolumen varierede fra et til tre sæt med to til fire gentagelser, udført med en intensitet, der oversteg 80 % af det maksimale antal gentagelser (1 RM), som blev genberegnet hver måned. Sessionerne varede ca. 10 minutter, og holdetiden blev valgt ud fra dokumentation, der viser, at patellarsenespændingen falder med ca. 60 % inden for 30 sekunder efter en vedvarende kontraktion og kun marginalt derefter.
I løbet af den 18 måneder lange intervention var progressive stigninger i belastning og holdvarighed forbundet med forbedringer i styrke på tværs af alle opgaver med modstand (benforlængelse, benpres og spansk squat-hold). Magnetisk resonansbilleddannelse (MRI) ved baseline, 12 måneder og 18 måneder viste en reduktion i senens reaktivitet, øget senediameter ved midsubstansen og nedsat tykkelse ved den proksimale indføring - fund, der var i overensstemmelse med strukturel remodellering. Atleten rapporterede progressiv smertereduktion og var smertefri ved 18-måneders opfølgningen.
Disse observationer tyder på, at isometrisk træning, især når den kombineres med ernæringsstrategier, der understøtter kollagensyntese, kan fremme senetilpasning og symptomforbedring. Evidensen er dog fortsat begrænset til eksperimentelle studier og isolerede case-rapporter. Større kontrollerede forsøg er nødvendige for at bestemme effektiviteten og de optimale parametre for isometriske protokoller. Derudover varierer seneegenskaberne alt efter anatomisk placering, tværsnitsareal og mekanisk miljø, hvilket kan påvirke den viskoelastiske adfærd og passende belastningsstrategier. Som understreget i denne gennemgang afhænger vellykket rehabilitering sandsynligvis af, at der opnås en passende balance mellem underbelastning og overdreven belastning, hvilket understreger behovet for pålidelige kliniske værktøjer til at overvåge mekanisk belastning med henblik på senetilpasning.
Tal nørdet til mig
Selvom narrative reviews er underlagt iboende bias som f.eks. selektionsbias, giver dette review en vigtig biologisk kontekst, som kan hjælpe fysioterapeuter med bedre at forstå senestruktur og mekanobiologi i behandlingen af tendinopati. Viden om genetisk regulering, transkriptionsveje, aminosyredynamik og proteinombygning bidrager til en dybere forståelse af seneheling og -tilpasning, hvilket kan informere om rehabiliteringsstrategier. De fleste mekanistiske beviser stammer dog fra dyremodeller, og direkte ekstrapolering til menneskelig senepatologi er fortsat begrænset.
Mens der er behov for mere avancerede kliniske forsøg for at styrke evidensgrundlaget, vil den efterfølgende artikel i denne serie undersøge data fra et studie fra 2022, der undersøger en træningsprotokol med høj belastning, der har til formål at øge senens tværsnitsareal og forbedre smerte og funktion hos patienter med akillestendinopati.
Budskaber, der kan tages med hjem
- Sener er levende, adaptive væv. De reagerer på mekanisk belastning gennem cellulær signalering og matrixomdannelse. Mekaniske stimuli driver strukturel tilpasning - sener er ikke inaktive strukturer.
- Biomekanisk belastning er afgørende for tilpasning. Passende mekanisk stress fremmer senesundhed og remodellering, understøtter funktionel genopretning og strukturel forbedring gennem mekanisk belastning på senetilpasning.
- Stressafskærmning begrænser tilpasningen. Degenerative seneregioner kan blive aflastet, når sundere væv bærer det meste af den mekaniske belastning. Det reducerer den effektive mekaniske stimulering og kan hæmme restitutionen.
- Rehabilitering skal overvinde stressafskærmning. Belastningsstrategier bør sigte mod at overføre mekaniske kræfter til degenerativt væv og samtidig undgå overdreven belastning. Viskoelastiske egenskaber (stressrelaksation og krybning) giver et biomekanisk grundlag for kontrolleret, terapeutisk belastning.
- Afbalanceret belastning er nøglen. Sener kræver tilstrækkelig mekanisk stimulus til at tilpasse sig, men er sårbare over for underbelastning (som fastholder manglende brug) og overbelastning (som kan forværre symptomerne). Individualiseret, progressiv belastning er afgørende.
- Kliniske implikationer for fysioterapi. Genoptræningen bør fokusere på målbare og progressive belastningsstrategier, der genopretter den mekaniske stimulering af det syge væv og udnytter senernes tilpasningsevne.
- Næste skridt. Den kommende artikel vil omsætte disse biomekaniske principper til kliniske strategier ved at gennemgå træningsprotokoller med høj belastning og praktiske tilgange til optimering af senetilpasning, smertereduktion og funktionel genopretning ved tendinopati.
Denne ressource fra Physiotutors giver yderligere perspektiver på senebiologi og mekanobiologi og tilbyder klinisk relevant indsigt i senefunktion og -tilpasning.
Reference
VMO'S OG QUADS' ROLLE I PFP
Se dette GRATIS VIDEOFORELÆSNING I 2 DELE af knæsmerteeksperten Claire Robertson, som dissekerer litteraturen om emnet, og hvordan den påvirker klinisk praksis.